
| 装置 | 反应前装置的质量/g | 反应后装置的质量/g |
| B | M | N |
| C | m | n |
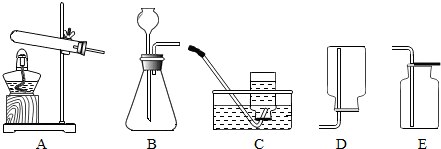
分析 (1)①根据用装置B来制备气体时需要的注意事项进行判断.
②根据H2、O2、CO2制取的装置进行分析,同时结合反应的原理进行分析.
③发生装置的选择与反应物的状态和反应的条件有关,收集装置的选择与气体的密度和溶解性有关,据此解答.
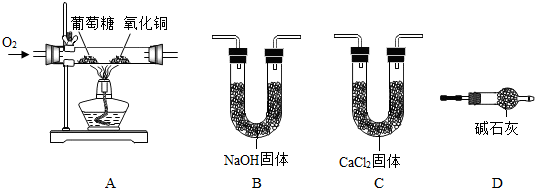
(2)①通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成,先吸收水,后吸收二氧化碳;
②C装置的质量增加是水的质量;
③装置D是为了防止空气中的二氧化碳和水分被装置C吸收,使测定结果偏高.
解答 解:(1)①长颈漏斗的末端未伸到锥形瓶的底部,会导致生成的气体从长颈漏斗逸出;
②B装置属于固液在常温下反应制取气体,H2、O2、CO2都可以用B装置制取,三种气体中只有氢气难溶于水,密度比空气小,既可用排水法收集又可用向下排空气法来收集,锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
③实验室常用氯化铵和熟石灰的固体混合物在加热条件下制取氨气,因此需要加热,发生装置选A;收集氨气只能用向下排空气法收集,说明易溶于水且密度比空气小;
(2)①通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成,由于NaOH固体既能吸收水,又能吸收二氧化碳,所以先用CaCl2固体吸收水,后用NaOH固体吸收二氧化碳;
②C装置的质量增加是水的质量,所以反应中生成水的质量是n-m;
③装置D是为了防止空气中的二氧化碳和水分被装置C吸收,若实验不连接装置D,空气中的二氧化碳和水分被装置C吸收,导致测定结果偏高;
故答案为:(1)①长颈漏斗下端没有伸入到锥形瓶的底部;
②H2、O2、CO2; Zn+H2SO4═ZnSO4+H2↑;
③2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2;A; 易溶于水且密度比空气小;
(2)①CB;
②n-m;
③装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,物质成分的鉴定等,考查学生运用所学化学知识综合分析和解决实际问题的能力.要结合各种装置的作用和物质的性质细心分析.


科目:初中化学 来源: 题型:解答题
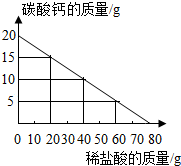 向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:
向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
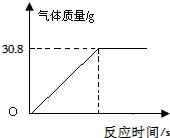 大理石(主要成分CaCO3)是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:
大理石(主要成分CaCO3)是重要的建筑材料.为了测定某大理石样品中杂质的含量,某实验小组准确称取100g样品,设计了如下实验方案:| 反应时间/min | 0 | 5 | 9 | 12 | 15 |
| 剩余固体质量/g | 100 | 91.2 | 73.6 | 64.8 | 64.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com