有关实验室制取氧气的实验,请结合图示装置回答下列问题:

(1)写出仪器名称:①
,②
(2)实验室用高锰酸钾制取氧气时,应选用的发生装置是
,(填字母,下同)你认为装置中还需添加
,否则可能会导致
,写出该反应的符号表达式:
.
如果要想得到一瓶干燥的氧气,还要选择的收集装置是:
.如用正放在空气中的F装置来收集氧气,则氧气从
端通入(填“a”或“b”).
(3)实验室用高锰酸钾制氧气主要过程为以下几步:①给试管加热;②检查装置气密性;③将试管固定在铁架台上;④装药品;⑤收集气体;⑥熄灭酒精灯;⑦将导管移出水面;
正确顺序为:
.
A.②④③①⑤⑥⑦B.④②③①⑤⑥⑦
C.④③②①⑤⑦⑥D.②④③①⑤⑦⑥
(4)如果选用B装置制取氧气,在锥形瓶中先放
(填物质状态),写出该反应的符号表达式
.
(5)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择
(填序号).甲烷气体一般采用装置E进行收集,收集满后集气瓶的放置方式如图2所示,据此可推断甲烷一定具备的物理性质是:
、
.
(6)某个兴趣小组同学对实验室制氧气的条件进行如下探究:
(a)为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
①将3.0g氯酸钾和1.0g二氧化锰均匀混合加热;
②将xg氯酸钾和1.0g氧化铜均匀混合加热.
在相同温度下,比较两组实验产生氧气的快慢.
①中反应的符号表达式是
;②中x的值应为
.
[猜想]除二氧化锰,氧化铜外,Fe
2O
3也可以做氯酸钾分解的催化剂.
按下表进行实验:测定分解温度(分解温度越低,催化效果越好)
| 实验编号 |
实验药品 |
分解温度/℃ |
| ① |
氯酸钾 |
580 |
| ② |
氯酸钾、二氧化锰(质量比1:1) |
350 |
| ③ |
氯酸钾、氧化铜(质量比1:1) |
370 |
| ④ |
氯酸钾、Fe2O3(质量比1:1) |
390 |
由实验
与实验④对比,证明猜想合理.实验所用的三种金属氧化物,催化效果最好的是
.
(b)乙探究了影响过氧化氢溶液分解速率的某种因素.实验记录如下:
|
过氧化氢溶液的质量 |
过氧化氢的浓度 |
二氧化锰的质量 |
相同时间内产生VO2 |
| ① |
50.0g |
1% |
0.1g |
9mL |
| ② |
50.0g |
2% |
0.1g |
16mL |
| ③ |
50.0g |
4% |
0.1g |
31mL |
实验结论:在相同条件下,
,过氧化氢分解得越快.
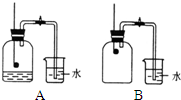
本实验中测量O
2体积的装置(如图)应该选择:
.(填字母)



 春雨教育同步作文系列答案
春雨教育同步作文系列答案
