
随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。
(1)在汽车电路中,经常用铜做导线,这是利用了铜的__ _性。
(2)车体多用铜材制造,其表面喷漆不仅美观,而且可有效防止与__ __接触而生锈。
(3)工业上用CO还原赤铁矿冶炼金属铁的化学方程式为___。
(4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是__ __。(填一种即可)
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:
下列是初中化学的三个实验,按要求回答问题。
 |
(1)实验C中烧杯③的作用是 。
(2)上述不能达到实验目的实验是 (填序号)。为实现相应实验目的,该实验改进的方法是  。
。
(3)实验A的实验原理是 ,
若实验测定出的空气中氧气的含量小于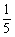 ,则造成的原因可能是
,则造成的原因可能是
、 。(写出两点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列用化学方程式表示的除杂(括号内为杂质)方法正确的是( )
|
B.CO2(CO):2CO+O2 === 2CO2
|
 C
C .N2(O2):2Cu+O2 === 2CuO
.N2(O2):2Cu+O2 === 2CuO 
 D.KCl (KClO3):2KClO3 === 2KCl+3O2
D.KCl (KClO3):2KClO3 === 2KCl+3O2
查看答案和解析>>
科目:初中化学 来源: 题型:
甲 乙两同学用不同方法测定A、B两种磁铁矿中Fe3O4的质
乙两同学用不同方法测定A、B两种磁铁矿中Fe3O4的质 量分数。(反应过程中所有杂质均不参与反应,计算结果均保留一位小数)
量分数。(反应过程中所有杂质均不参与反应,计算结果均保留一位小数)
(1)甲同学取8gA种磁铁矿于玻璃 管中,通入足量的CO,并在不同时刻测定管内剩余固体的质量(如下表):
管中,通入足量的CO,并在不同时刻测定管内剩余固体的质量(如下表):
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量/g | 7.6 | 7.0 | 6.4 | 6.4 |
①该种磁铁矿中Fe3O4的质量分数为 。
②t2时,固体混合物中铁元素的质量分数为 。
(2)乙同学获知若1500tB种磁铁矿用于工业炼铁,最多可得到含杂质4%的生铁875t,
求B种磁铁矿中Fe3O4的质量分数。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
下列关于铁制品的使用合理的是()
A.铁桶加入硫酸铜溶液和石灰水配制农药
B.菜刀用湿布包起来防止生锈
C.不锈钢可用于制作外科手术刀
D.用铁锅长期存放姜醋
查看答案和解析>>
科目:初中化学 来源: 题型:
开发和利用清洁而又高效的新能源,是21世纪人类面临的重要课题。
(1)氢气是未来最理想的能源,理想的制氢方法是
。目前已经开发利用的氢氧燃料电池是一种将 能转化为电能的装置。
(2)目前,烟台市长岛、栖霞、莱州、招远、开发区等地的风力发电厂已经建成或正在建设中;海阳的核电项目也已经启动。这些新能源的利用和开发除了促进经济发展外,你认为还有哪些好处(写出两条)?
;
。
查看答案和解析>>
科目:初中化学 来源: 题型:
高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
(1)试管尾部放一团湿棉花的目的是 。
(2)探究生成的气体是什么? 用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是______________。写出该反应的化学方程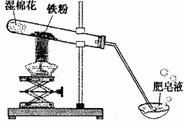 式 。
式 。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 与盐酸反应 | FeCl2+H2O | FeCl3+H2O | FeCl2+ FeCl3+H2O |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是 ;猜想二:剩余固体________。
【实验探究】(每空2分)
| 实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为_______________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
(4)若反应前称得铁的质量为2.1g,高温下,铁与水反应结束称得固体质量为2.8 g则剩余固体成分是 。(通过计算说明,要求写出计算过程)
g则剩余固体成分是 。(通过计算说明,要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
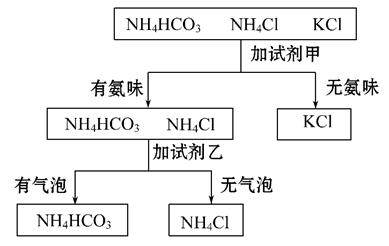
某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥。过程如图所示,其中试 剂甲和乙可能是( )
剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:稀硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com