
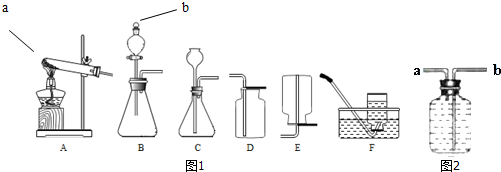
分析 (1)据常用仪器回答;
(2)停止加热时,应先移导管后熄灯,防止水倒吸引起试管炸裂;验满氧气的方法是将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(3)收集一瓶氧气后,用带火星的木条伸到瓶口、瓶内、瓶底都未见木条复燃,可能装置漏气,未收集到氧气;
(4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置;收集干燥的气体用排空气法,收集纯净的气体用排水法,据反应原理书写表达式;
(5)过氧化氢制取 氧气不需加热,节约能源,且操作简单、安全;
(6)在常温下用块状电石与水反应制取乙炔,属于固液常温型,因为反应必须严格控制加水速度,以免剧烈反应反应引起发生装置炸裂,分液漏斗可逐滴滴加液体,控制反应速率,并据乙炔性质性质收集方法;乙炔密度比水小,所以应从短管进气,长管便于排水.
解答 解:(1)标号仪器分别是试管和分液漏斗;
(2)用加热氯酸钾的方法制取并取用排水法收集氧气,停止加热时,应先将导管移除水面,后熄灭酒精灯,防止水倒吸引起试管炸裂;验满氧气的方法是将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(3)收集一瓶氧气,用带火星的木条伸到瓶口、瓶内、瓶底都未见木条复燃,其原因是装置漏气,如果装置漏气,收集的氧气不纯,或收集不到氧气,从而导致带火星的木条不能复燃;
(4)用高锰酸钾为原料制取氧气需要加热,属于固体加热型,故选发生装置A,氧气密度比空气大,所以要收集一瓶干燥的氧气可用向上排空气法;
用过氧化氢溶液和二氧化锰制取氧气属于固液常温型,可选发生装置BC,B装置中的分液漏斗可以控制滴加液体的速度,从而得到平稳的氧气流,氧气不易溶于水,所以收集纯净的氧气用排水法;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的文字表达式是:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(5)用过氧化氢制取氧气的优点是不需要加热,节约能源,且操作简单、安全;
(6)在常温下用块状电石与水反应制取乙炔,属于固液常温型,可以用B或C装置作为发生装置,B装置中的分液漏斗可以控制水的流量,从而可以控制反应速率,因此图1中最适合制取乙炔气体的发生装置是B装置,乙炔密度比空气大,微溶于水,所以用向上排空气法收集;
如果用如图2所示装置收集乙炔,气体应从b端管口通入,长管便于排水;
故答案为:(1)试管;分液漏斗;
(2)熄灭酒精灯;将带火星的木条放于集气瓶口,若木条复燃则收集满了;
(3)装置漏气;
(4)AD;BF;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(5)小华;不需要加热,操作简单、安全(合理均可);
(6)B;D;b.
点评 了解制取氧气的反应原理、选取方法、氧气的验满等知识,并能对装置进行简单分析和评价,较好考查了学生分析、解决问题的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | B. | 4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | 2KMnO4═K2MnO4+MnO2+O2↑ | D. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 次氯酸钠中氯元素的化合价为-1 | |
| B. | 次氯酸钠是氧化物 | |
| C. | 过氧乙酸由三个元素组成 | |
| D. | 过氧乙酸中碳、氢、氧元素的原子个数比为2:4:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com