
| 装置C/g | 装置D/g | 装置E/g | |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
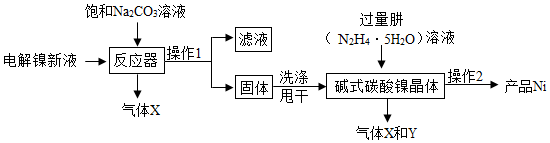
解答 解:I、【镍粉制备】:工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:
(1)反应器中一个重要反应为 3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,根据质量守恒定律可推得X的化学式为 CO2.
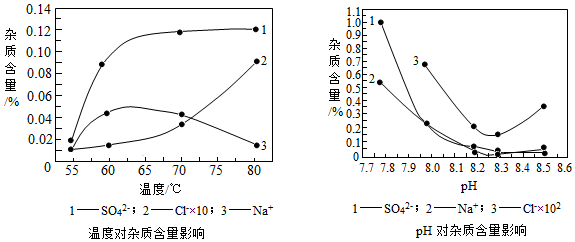
(2)根据给出的温度和pH对杂质含量的影响图可知,要想杂质含量最低,则需要控制反应器中最适合的温度及pH分别为 55℃、8.3.
(3)由于NiCO3中含镍量比Ni(OH)2中低,生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,而Ni(OH)2中含镍量高,所以会造成生成的碱式碳酸镍晶体中,镍的含量将升高.
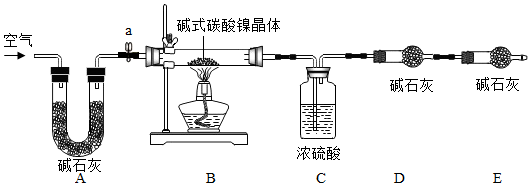
Ⅱ.【测定碱式碳酸镍晶体的组成】由于需要测定过程中生成的二氧化碳和水的质量,所以需要装置的气密性良好,而过程中生成的二氧化碳和水都要被吸收后才能测定其质量,所以反应完毕后要通入不含水蒸气和二氧化碳的空气以便使生成的二氧化碳和水蒸气被装置C和装置D完全吸收,减小误差.
(4)所以实验步骤中的填空:①检查装置的气密性;⑤鼓入空气.
(5)装置E的作用是 装置右侧的空气进入装置内造成干扰;
(6)由表可知生成的水的质量为201.08g-200.00g=1.08g,而二氧化碳的质量为180.44g-180.00g=0.44g.由于是分解反应,所以可知固体的质量为3.77g-10.8g-0.44g=2.25g.根据信息可知碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.得如下化学方程式和质量关系
xNiCO3•yNi(OH)2•zH2O$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)NiO+xCO2↑+(y+z)H2O
75(x+y) 44x 18(y+z)
2.25g 0.44g 1.08g
$\frac{75(x+y)}{44x}$=$\frac{2.25g}{0.44g}$ 得 y=x
$\frac{44x}{18(y+z)}$=$\frac{0.44g}{1.08g}$ 得4y=z
计算 xNiCO3•yNi(OH)2•zH2O中x:y:z=1:1:4.
【实验反思】:
(7)实验结束后,称得装置B中残留固体质量为2.33g.而生成NiO的时候只生成2.25g,由于镍元素质量不变,所以应该是400℃左右,NiO会氧化生成Ni2O3.所以该固体为NiO和Ni2O3的混合物.
设混合物中Ni2O3 的质量为x.
根据关系式
2NiO∽∽∽Ni2O3 固体质量增加量
150 166 166-150=16
x 2.33g-2.25g=0.08g
$\frac{166}{16}$=$\frac{x}{0.08g}$
x=0.83g
则NiO的质量为2.33g-0.83g=1.50g
故答案为:
I、【镍粉制备】
(1)CO2.
(2)55; 8.3.
(3)升高.
Ⅱ.【测定碱式碳酸镍晶体的组成】:
(4)①检查装置的气密性;⑤鼓入空气.
(5)装置右侧的空气进入装置内造成干扰;
(6)1:1:4.
(7)NiO和Ni2O3混合物,其中NiO的质量为1.50g而Ni2O3的质量为0.83g..
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.


科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的废液于试管中,向其中加入Na2CO3溶液至过量 | 只有白色沉淀生成 | 猜想Ⅰ正确 |
| 先气泡产生 后白色沉淀生成 | 猜想Ⅱ正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 市场上有“葡萄糖酸锌”、“家铁酱油”等商品,这里的锌,铁是指元素 | |
| B. | 用一种高效的催化剂可把水变成汽油 | |
| C. | 蚊虫叮咬后,会在人的皮肤内分泌蚁酸使皮肤肿痛,可涂点醋酸来减轻痛痒 | |
| D. | 长期饮用纯净水对健康有利 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 高锰酸钾 | 熟石灰 | 纯碱 |
| 化学式 | KMnO4 | Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| C. | 铁钉放入硫酸铜溶液中,其表面产生红色固体 | |
| D. | 生石灰与水反应吸收热量,导致周围温度降低 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单质是由一种元素组成的,因此由一种元素组成的纯净物一定是单质 | |
| B. | 中和反应一定有盐生成,则有盐生成的反应一定是中和反应 | |
| C. | 分子是构成物质的微粒,因此物质都是由分子构成的 | |
| D. | 氧化物中含有氧元素,因此含有氧元素的化合物一定是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com