
【题目】碳的耗用量称为“碳足迹”。一般情况下,排放的二氧化碳较多,碳足迹就越大.以下做饭可以减小“碳足迹”的是( )

A. 大量使用煤、石油等燃料 B. 减少一次性筷子的使用
C. 将生活垃圾进行焚烧处理 D. 以私家车出行代替公共交通工具
科目:初中化学 来源: 题型:
【题目】结合图示实验装置,回答下列问题。
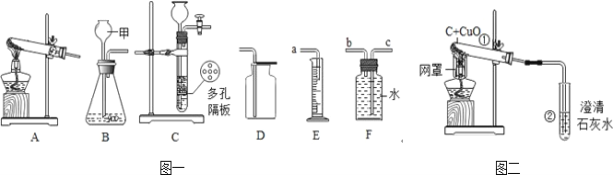
(1)实验室加热高锰酸钾制取氧气应选用的发生装置为___________(填字母),试管中棉花的作用是______________。
(2)若选B装置作为实验室制取氧气的发生装置,反应的化学方程式为:___________,某同学用D装置收集氧气,验满方法是___________。
(3)实验室可用B或C装置制二氧化碳,选用C相对于B装置的主要优点是___________。
(4)某同学用E、F装置收集一定量的氧气,装置接口连接的顺序为___________(填接口字母),量筒的作用是___________。
(5)图二中,酒精灯加网罩的目的___________。试管①中发生反应的化学方程式为:___________。
(6)图二实验停止加热时,应先将导管从试管②中撤出,并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出,这样操作的原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某粒子的结构示意图,下列有关该粒子的说法错误的是
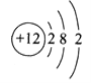
A. 该粒子的原子核内有12个质子
B. 该粒子带12个单位的正电荷
C. 该粒子的原子核外有3个电子层
D. 该粒子在化学反应中易失去2个电子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验.
(1)同学们按如图装置进行实验,实验前先检查装置的__,要将炭粉和氧化铜粉末充分混合后再装入试管中,这样做的目的:__;当看到澄清的石灰水刚刚出现浑浊时,__________(填写“可以”或者“不能”)确定氧化铜和炭粉已经开始反应.
(2)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例,你建议选择__(填写字母),简要说明你的理由__________.
A.36:3 B.40:3 C.48:3.

(3)研究发现:物质的结构决定性质,物质的性质决定用途。如:一氧化碳也能还原氧化铜,也有还原性。从化学反应前后碳元素化合价的变化特点分析,一氧化碳和碳都具有还原性的原因是__;而二氧化碳没有还原性的原因是__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式。
(1)电解水____; (2)用石灰水检验二氧化碳____;
(3)铁和稀盐酸反应____; (4)铝和氧气反应____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是实验常用仪器的装置图,请按要求填空:
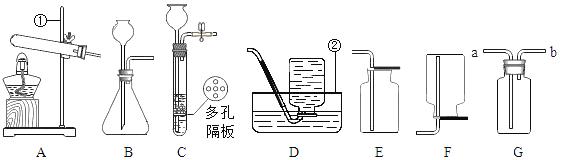
(1)写出标号仪器名称:①___________、②___________;
(2)某同学在实验室用装置C(多孔隔板用来放块状固体)制取CO2,装置C与装置B相比,其优点为_______________;
(3)若将装置G装满水,排水法收集O2,O2应由________(填“a”或“b”)端进入;
(4)用装置D收集氧气时,观察到____________的现象时,表明氧气已收集满;
(5)在标准状况下,氨气(NH3)的密度约为0.8g/L,空气的密度约为l.3g/L,且l体积水能溶解700体积的氨气。在实验室中,常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,反应同时会产生氯化钙和水。则选用的发生装置和收集装置是_______(填序号,在A~F之间选择),该反应的化学方程式是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源。煤气化和液化流程示意图如下图所示,请结合图像回答问题:
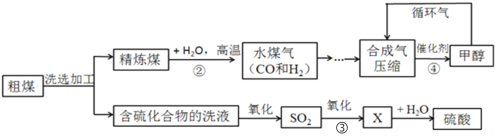
(1)精炼煤中主要成分是碳,步骤②中发生反应的化学方程式为__________。
(2)步骤③中,SO2进一步氧化得到X,X为硫的另一种氧化物,其中硫元素的化合价为+6价,X的化学式为________。
(3)经过进一步净化,含较多杂质的水煤气转化为合成气(CO和H2的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的化学方程式为_________,该反应的基本类型是 _________。
(4)循环气的主要成分是__________和少量未完全分离出去的甲醇。
(5)从“绿色化学”的角度分析,“煤的气化和液化”流程的优点:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示。边回答:
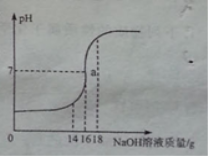
(1)a点溶液中大量存在的离子有______________。
(2)当恰好完全反应时,消耗NaOH溶液的质量为__________。
(3)计算稀盐酸中溶质的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com