氢化钙(CaH
2)是一种常用的储氢材料,也是登山运动员常用的能源提供剂.
【资料在线】
Ⅰ.金属钙的活动性很强,遇水即刻剧烈反应生成氢氧化钙,同时产生一种气体.
Ⅱ.氢化钙要密封保存,一旦接触到水就发生反应,放出氢气.
Ⅲ.用氢气与金属钙加热的方法可制得氢化钙.
Ⅳ.白色的无水硫酸铜粉末吸水后会变蓝.
探究一:定性分析
(1)对于“金属钙与水反应生成的气体”有如下猜想:甲.氧气,乙.氢气你支持
乙
乙
(填“甲”、“乙”)观点,理由是
钙与水反应若生成氧气,反应前后氢氧原子个数比不守恒(反应前氢氧原子个数比为2/1,反应后会大于2/1)
钙与水反应若生成氧气,反应前后氢氧原子个数比不守恒(反应前氢氧原子个数比为2/1,反应后会大于2/1)
.
(2)CaH
2中氢元素的化合价是
-1
-1
,写出CaH
2与水反应的化学方程式
CaH2+2H2O═Ca(OH)2+2H2↑
CaH2+2H2O═Ca(OH)2+2H2↑
;
(3)登山运动员常携带氢化钙作为能源提供剂,与携带氢气相比,其优点是
固体燃料携带方便,且水是登山运动员必须携带物质,有水就能提供出高能量的氢能
固体燃料携带方便,且水是登山运动员必须携带物质,有水就能提供出高能量的氢能
;
(4)用氢气与金属钙加热可得到氢化钙,以下是反应装置图.
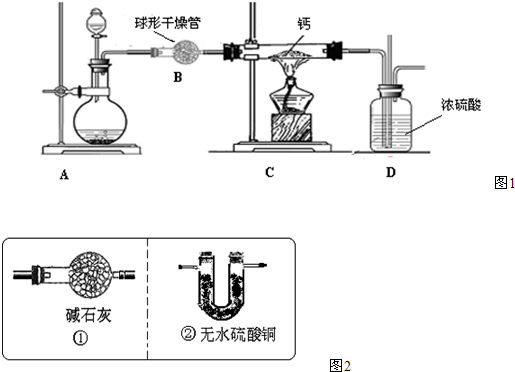
装置A 中装有锌粒和稀硫酸,请写出其反应的化学方程式
Zn+H2SO4═ZnSO4+H2↑;
Zn+H2SO4═ZnSO4+H2↑;
,装置B 中装有无水氯化钙,其作用是
除去氢气中混有的水蒸气
除去氢气中混有的水蒸气
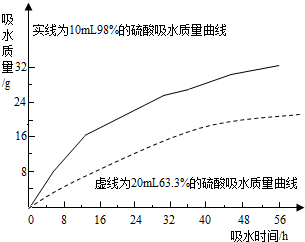
,若要证明进入C 装置中的氢气已经干燥,在B、C之间应连接下图中的哪个装置:
②
②
(填①或②),现象是
无水硫酸铜不变色
无水硫酸铜不变色
.
(5)制备CaH
2实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,在溶液中滴入酚酞后显红色.该同学据此判断:上述实验确有CaH
2生成.你认为是否正确
否
否
(填“是”或“否”);原因是
因为Ca+2H2O═Ca(OH)2+H2↑也能呈现相同的现象
因为Ca+2H2O═Ca(OH)2+H2↑也能呈现相同的现象
.
探究二:产物定量测定
测定原理:根据金属钙、氢化钙都能与水反应生成气体的原理,采用测定气体的体积的方法.
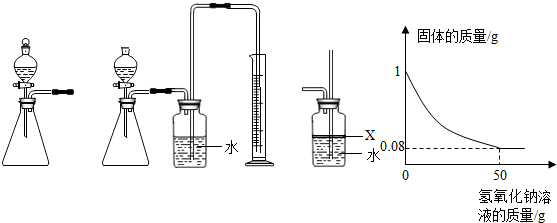
(1)取氢化钙样品与水反应,利用图1装置测定生成的气体体积时,在
B
B
即进行收集(填字母).
A.气泡连续均匀时
B.刚开始有气泡时
(2)利用该装置,测得的气体体积总是会偏小,同学讨论后采用图2装置测定气体体积.该装置的优点是
①排除了“因液体加入引起气体排出导致的气体体积测定误差”的可能;②避免了实验操作时,无论塞紧橡皮塞的动作多快,都会有气体逸散的可能;③胶皮管能使两支管内中气体压强保持平衡,便于管A中液体顺利流入管B;④评价气球:气球膨胀过程还可以在一定程度上缓冲一下压强,以防氢气直接快速进入注射器,造成活塞脱落,导致实验失败
①排除了“因液体加入引起气体排出导致的气体体积测定误差”的可能;②避免了实验操作时,无论塞紧橡皮塞的动作多快,都会有气体逸散的可能;③胶皮管能使两支管内中气体压强保持平衡,便于管A中液体顺利流入管B;④评价气球:气球膨胀过程还可以在一定程度上缓冲一下压强,以防氢气直接快速进入注射器,造成活塞脱落,导致实验失败
,如何实现A中的水与B中样品接触而发生反应
因为AB管连接处均有胶皮管连接,所以慢慢倾斜A管,直至液体流入B
因为AB管连接处均有胶皮管连接,所以慢慢倾斜A管,直至液体流入B
.
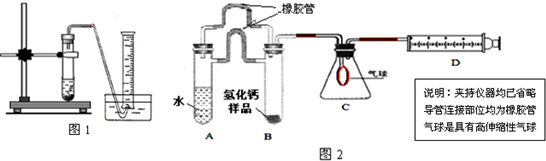
(3)称取46mg 所制得的氢化钙样品,注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处.试通过计算求出样品中氢化钙的纯度(即氢化钙在样品中的质量分数)是
91.30%
91.30%
.(设该条件下每11.2mL氢气的质量为1mg)
反思提高:
(1)上述实验在学校的实验室内,通过托盘天平等称量工具
不能
不能
(填“能”、“不能”)完成.
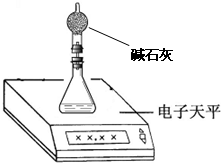
(2)测量小组利用电子天平,采用如下图所示方法以反应前后失去的质量来求算纯度,结果纯度的测定值偏
偏低
偏低
.

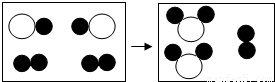
 分子,即一种物质,故该反应符合“多变一”的化合反应特征;
分子,即一种物质,故该反应符合“多变一”的化合反应特征;

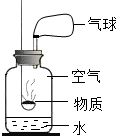 某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.
某校化学兴趣小组同学做镁带在空气中燃烧的实验时,发现白色生成物中混有少量淡黄色固体.针对这一现象,他们开展了如下实验探究.请仔细阅读并完成下列探究报告.