
【题目】如图,为某学习小组探究金属化学性质时所做的四个实验,仔细分析回答下列问题:

(1)实验前用砂纸打磨金属的目的是_______________;
(2)D中除了观察到铁的表面有气泡产生外,还能观察到反应后的溶液呈________,铁与稀硫酸恰好完全反应后溶液中的溶质是____________;
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是_________(填序号),由此判断出三种金属的活动性由强到弱的顺序是_______________;
(4)除去铜粉中的少量铁粉可以用___________溶液.
【答案】除去金属表面的氧化层,使金属充分接触溶液 浅绿色 FeSO4 A、B Fe>Cu>Ag 硫酸铜
【解析】
(1)金属表面可有存在氧化薄膜层,用砂纸打磨能除去氧化层,使金属与溶液充分接触
(2)铁与稀硫酸反应生成硫酸亚铁和氢气,方程式为H2SO4+Fe=FeSO4+H2↑,且Fe2+为浅绿色
(3)要确定Cu、Fe、Ag的活动性顺序,要能知道铜能否置换银,银能否置换铁,铁能否置换铜。因此只用A和B就能确定Cu>Ag和Fe>Cu,所以活动性Fe>Cu>Ag
(4)D实验证明Fe能与硫酸铜溶液反应,因此可用硫酸铜溶液除去Cu中混的少量Fe
故答案为:除去金属表面的氧化层,使金属充分接触溶液;浅绿色;FeSO4;A、B;Fe>Cu>Ag;硫酸铜


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源: 题型:
【题目】下列指定反应的化学方程式正确的是( )
A. 铝粉溶于稀盐酸:Al+2HCl=AlCl2+H2![]()
B. 用双氧水制氧气:H2O2![]() H2
H2![]() +O2
+O2![]()
C. 电解饱和食盐水生产烧碱和氯气:2NaCl+2H2O![]() 2NaOH+H2
2NaOH+H2![]() +Cl2
+Cl2![]()
D. 小苏打治疗胃酸过多:NaHCO3+H2SO4=Na2SO4+H2O+CO2![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中“![]() ”“
”“![]() ”“
”“![]() ”分别表示甲、乙、丙三种不同的分子,请根据图示回答下列问题。
”分别表示甲、乙、丙三种不同的分子,请根据图示回答下列问题。
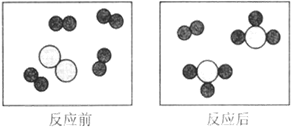
(1)参加反应的甲和乙的分子个数比是_____。
(2)一个丙分子由_____个原子构成;由大量丙分子聚集成的丙物质_____(填“可能”或“不可能”)是氧化物。
(3)该反应的基本反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映其对应操作的是( )

A.一定量的NaOH溶液中逐滴加入稀盐酸
B.等质量、等质量分数的稀硫酸中分别加入足量的镁粉和锌粉
C.用适量KClO3和MnO2的混合物加热制取O2
D.等质量、不同形状的石灰石中分別加入足量相同的稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,相信你已经掌握了一些化学知识与实验探究能力。
Ⅰ.请结合下列实验装置图回答问题。
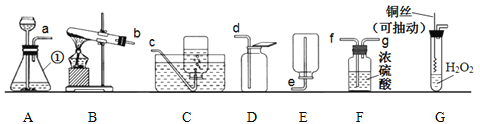
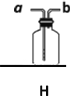
(1)写出图中①的仪器名称:_______________。
(2)实验室用过氧化氢制取氧气的化学方程式为_______________,实验室用此反应原理制取并收集一瓶干燥的氧气,应选用的装置连接顺序为_______________ (选填小写字母).
(3)查阅资料:氧化铜可以用作过氧化氢分解制氧气的催化剂。现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经加热处理。改进后发生装置如图G所示(已略去夹持装置)。
①铜丝绕成螺旋状的作用是____________(填序号)。
A 收集到更多的氧气 B 加快反应速率 C 没有影响
②与装置A比较,改进后装置的优点是______________。
Ⅱ.过氧化钠(Na2O2)是淡黄色固体,保存不当会变质而发白色。化学兴趣小组查得以下资料,对于过氧化钠变质的原理,有两种不同的原因:
甲:2Na2O2 + 2CO2 ═ 2Na2CO3 + O2
乙:2Na2O2 + 2H2O ═ 4NaOH + O2↑
为探究过氧化钠变质原理的合理性,开展以下实验:
(实验过程)
[实验1]取适量保存不当而变质发白色的固体于试管中,加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
(1)石灰水变浑浊的原因是__________(用化学方程式表示)。
(2)化学兴趣小组认为:据此现象,还不能得出“反应甲是造成过氧化钠变质的原因”的结论。理由是______________。
[实验2]兴趣小组设计了如图的实验装置,探究二氧化碳与过氧化钠反应。B中盛有饱和碳酸氢钠溶液,可除去二氧化碳中混有的________________ 气体。方程式为_________
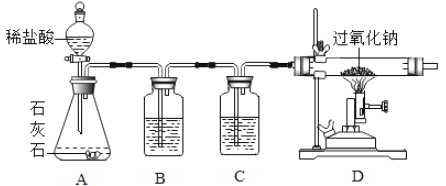
(3)C中盛有浓硫酸,其作用是__________。
(4)在D中观察到______________现象时,说明二氧化碳与过氧化钠发生了化学反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是 A、B、C 三种物质的溶解度曲线,请认真分析并回答:
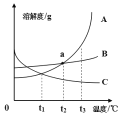
(1)t3℃时,A、B、C 三种物质的溶解度由小到大的顺序为_____。
(2)a点的含义是__________。
(3)t2℃时,A、B、C 三种物质的饱和溶液降温到 t1 ℃时变为不饱和溶液的是_____。
(4)当B中含有少量的 A,可采用______(填“降温”或“蒸发”)结晶的方法提纯 B 物质。
(5)t3℃时,若用 A、B 两物质各50g配成饱和溶液,则所需加水的质量 A_____B(填 “>”、“<”、“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室常用的实验仪器。请回答以下问题:
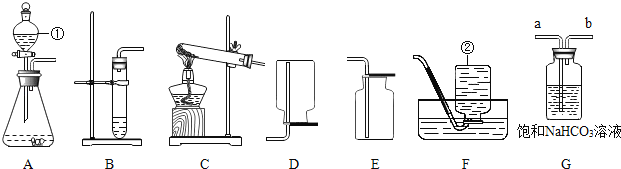
(1)写出标有序号的仪器的名称:①_____;②_____。
(2)若选择C装置制取氧气,反应的化学方程式为_____。若用锌粒和稀硫酸制取氢气(通常状况下,氢气是一种无色无味的气体,密度比空气小,难溶于水,也不与水反应)。应选择_____(填图中字母序号)作为收集装置。
(3)实验室制取的CO2中常混有水蒸气和从盐酸中挥发出来的少量HCl气体,现用G装置可除去混有的HCl气体。则除杂时应将气体从_____(填“a”或“b”)导管通入。若要得到干燥纯净的CO2气体,干燥装置应安装在装置G_____(填“前”或“后”)。
(4)为比较CO2和空气的温室效应,可将盛满两种气体的密闭集气瓶同时置于阳光下进行实验,此实验需定时测量的数据是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案中,不能达到实验目的的是
A. 测定空气中氧气含量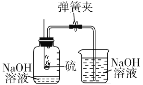
B. 比较可燃物的着火点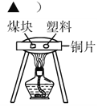
C. 验证质量守恒定律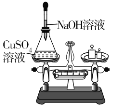
D. 证明铁生锈是水和氧气共同作用的结果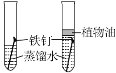
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组做镁条在空气中燃烧实验时,发现生成物中有黑色固体。针对这一现象,该小组同学猜想可能是镁与N2或CO2反应生成黑色固体。于是他们设计以下实验探究活动:
(提出猜想)猜想I:镁在空气中燃烧产生的黑色固体是镁与N2反应生成的。
猜想Ⅱ:镁在空气中燃烧产生的黑色固体是镁与CO2反应生成的。
(实验一)镁带与氮气的反应
(1)以下是获取氮气的方法及装置,其中得到氮气较纯的是_______(填字母)
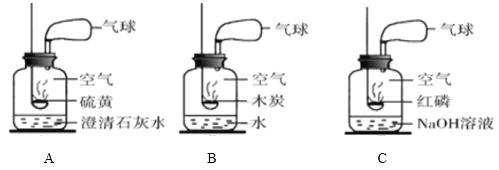
(2)燃烧镁带,观察现象:将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,瓶内壁附着一层淡黄色的固体。
(3)实验结论:镁与氮气在点燃的条件下发生化学反应,生成淡黄色的______(用化学式表示)。
(4)实验反思:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁?原因是__________。
(实验二)镁带与二氧化碳的反应
将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内产生氧化镁和一种黑色固体单质,该反应的化学方程式是________。
(探究结论)通过实验可以得出猜想________是正确的。
(反思交流)小组同学通过以上实验发现镁在二氧化碳中也能燃烧,由此他们认为燃烧并不一定需要______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com