
分析 (1)根据能跟酸反应,生成盐和水的氧化物,叫做碱性氧化物考虑;(2)根据偏铝酸钠的构成分析,(3)两性氧化物就是既能给酸反应,也能给碱反应生成盐和水的氧化物.
解答 解:(1)氧化铁能与酸反应生成铁盐和水,所以氧化铁属于碱性氧化物,水、一氧化碳、二氧化碳都不能与酸反应,故选D;
(2)偏铝酸钠由钠离子和偏铝酸根离子构成,所以属于盐,电离时产生的阴离子是AlO2-.
(3)由信息可知,既能跟碱反应生成盐和水,又能跟酸反应生成盐和水的氧化物属于两性氧化物.
故答案为:(1)D;(2)盐;AlO2-;(3)即可以和酸反应又可以碱反应,生成盐和水的氧化物.
点评 解答本题关键是从题干中提取有用信息,并能灵活运用.


科目:初中化学 来源: 题型:解答题
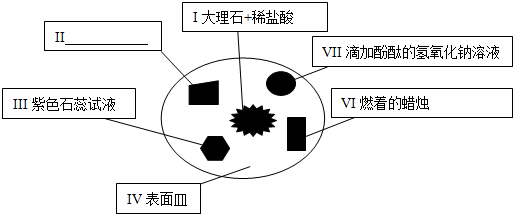
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
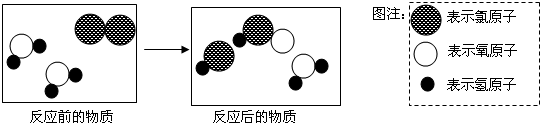
| A. | 化学反应的实质是分子破裂和原子的重新组合 | |
| B. | 生成物中有三种不同的分子 | |
| C. | 反应物中无单质 | |
| D. | 反应前后元素化合价均无变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钠用于治疗胃酸过多 | B. | 纯碱溶液用于洗去钢板表面的油污 | ||
| C. | 食醋用于除去热水瓶胆内的水垢 | D. | 生铁用于制造炒菜的锅 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE(-[CH2-CH2-CF2-CF2]n-)膜,并采用新一代的氮化镓高亮度LED材料.下列说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE(-[CH2-CH2-CF2-CF2]n-)膜,并采用新一代的氮化镓高亮度LED材料.下列说法正确的是( )| A. | 钒氮合金高新钢属于混合物 | |
| B. | 合金的熔点通常比成分金属高,硬度比成分金属小 | |
| C. | ETFE膜是一种易降解的有机高分子材料 | |
| D. | 已知镓(Ga)元素在化合物中显+3价,可推知氧化镓化学式为GaO |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
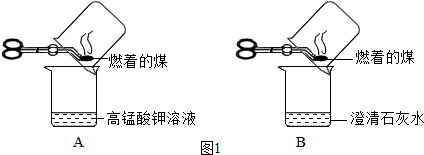
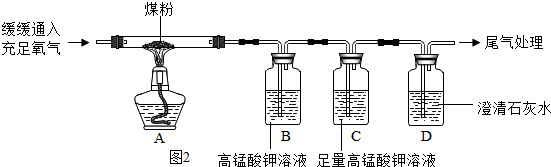
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com