
| A. | 由钙、碳、氧三个元素组成 | B. | 碳元素的化合价为+2 | ||
| C. | 钙元素的质量分数为40% | D. | 属于氧化物 |
分析 A.根据元素的规定来分析;
B.根据化合物中元素化合价的计算方法来分析;
C.根据化合物中元素质量分数的计算方法来分析;
D.根据氧化物的概念来分析.
解答 解:A.碳酸钙是由碳、氢、氧三种元素组成的,元素是个宏观概念,只讲种类、不讲个数,故错误;
B.碳酸钙中,钙元素显+2价,氧元素显-2价,设其中钙元素的化合价为x,则(+2)+x+(-2)×3=+4,故错误;
C.碳酸钙中,钙元素的质量分数为:$\frac{40}{40+12+16×3}×100%$=40%,故正确;
D.氧化物是由两种元素组成的,而碳酸钙中含有三种元素,故错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
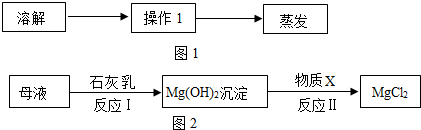
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | t2℃时,三种物质的饱和溶液中A溶液的溶质质量分数最大 | |
| B. | t1℃时,三种物质的溶解度由大到小的顺序为:B>A=C | |
| C. | 要将C的接近饱和的溶液转化为饱和溶液可以采用升温的方法 | |
| D. | A中混有少量B,可采用冷却热饱和溶液的方法提纯A |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
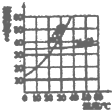 根据如图KNO3和 NaCl两种由体物质的溶解度曲线.回答下列问题.
根据如图KNO3和 NaCl两种由体物质的溶解度曲线.回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将不饱和溶液变为饱和溶液不能采用升高温度的方法 | |
| B. | 将10g食盐溶解在100g水中,所得溶液的溶质质量分数为10% | |
| C. | 将100g饱和的食盐溶液中取出的5g,则变为不饱和溶液 | |
| D. | 当溶液被水稀释时,溶液中保持不变的是溶质的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
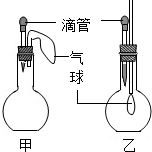 化学课上,老师将CO2分别通入澄清石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者没有明显现象,CO2和NaOH是否发生了化学反应呢?同学们对反应后的溶液进行探究.
化学课上,老师将CO2分别通入澄清石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者没有明显现象,CO2和NaOH是否发生了化学反应呢?同学们对反应后的溶液进行探究.| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 取反应后的溶液少许于试管 中,向试管中滴加几滴酚酞试液,振荡 | 若溶液变红,则猜想(2)(3)不成立 | 同学认为:此方案结论不正确,理由是碳酸钠溶液能使酚酞试液变红色. |
| 第2组 | 取反应后的溶液少许于试管中,向试管中加入足量的CaCl2(呈中性)溶液,振荡. | 若产生白色沉淀,反应方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl,则猜想(1)不成立. | 猜想(2)(3)尚无法确定其一. |
| 第3组 | 将第2组实验后的混合物过滤,向滤液中滴加氯化铜溶液 | 若无蓝色沉淀,则猜想(2)成立,若有蓝色沉淀,则猜想(3)成立. | 也可以用酚酞试液(填试剂名称)也能达到实验目的. |
| 符合装置乙实验现象的试剂组合为 | 胶头滴管内液体 | 瓶中物质 | |
| 1 | NaOH溶液或水 | CO2 | |
| 2 | 石灰水 | CO2 | |
| 3 | 水 | 氨气 | |
| 4 | NaOH溶液 | 氯化氢 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com