

| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
分析 方案一:(1)根据用pH试纸测定溶液的pH的方法进行分析;
(2)根据用盐酸滴定氢氧化钠溶液时,如果盐酸过量,则使溶液的pH小于7进行分析;
方案二:(1)根据氧气不易溶于水,所以空气中的氧气有一少部分会溶于水,加热可把水中的氧气除去;植物油浮在水面上,能防止氧气进入溶液进行分析;
(2)根据碳酸钠溶液显碱性进行分析;
(3)根据用稀释浓氢氧化钠溶液的方法检验浓氢氧化钠能使变红的酚酞试液的红色消失进行分析;
方案三:(1)根据表中的数据第一组与第三组的数据进行分析判断解答即可;
(2)根据中和反应是放热反应使烧瓶中的气体膨胀,压强变大的角度进行分析;
(3)①根据胶头滴管的用途进行分析;
②根据玻璃棒的作用进行分析;
③根据碳酸钠与盐酸反应的现象进行分析;
④根据氢氧化钠与二氧化碳的反应情况进行分析;
(4)根据该题中所发生的化学反应,可以知道是碳酸钠和盐酸的反应,然后依据二氧化碳气体的质量来求出碳酸钠的质量,然后判断是否有氢氧化钠进而解答该题.
解答 解:方案一:(1)用pH试纸测定溶液的pH时,正确的操作是:将pH试纸放在表面皿上,用玻璃棒蘸取少量待测液滴在试纸上,将试纸颜色与比色卡对照读出pH值;
(2)向NaOH溶液中再滴加盐酸,如果盐酸过量,这时溶液呈酸性,溶液的pH小于7;
方案二:(1)由于水中溶有少量的氧气,加热是为了除去溶液中的氧气,滴加植物油是为了防止空气中的氧气进入;
(2)碳酸钠虽然是盐,但它的水溶液显碱性;
(3)可以采用向浓氢氧化钠溶液中加水稀释的方法来证明,所以①实验方法:向氢氧化钠溶液中滴几滴酚酞试液,可观察到溶液先变红色,过一会红色消失,再向溶液中加入水进行稀释,观察现象,②观察到的现象:溶液又变成红色;
方案三:(1)第三组中氢氧化钠和盐酸的浓度都是第一组的2倍,浓度叠加就是第一组的4倍,温度的变化是第一组的4倍;第二组与第一组比较,盐酸的质量分数不变,而氢氧化钠的浓度是第一组的2倍,所以温度的改变也是第一组的2倍,所以X的值是7;
(2)氢氧化钠和盐酸发生中和反应,溶液的温度会升高,导致烧瓶内的压强增大,使U形管的液面出现高度差,所以U形管中的液面左低右高;
(3)①在盐酸和氢氧化钠反应时,如果加入盐酸的速度稍快可能会使加入的盐酸过量,如使用胶头滴管加入盐酸,可以防止稀盐酸过量;
②用玻璃棒搅拌能够使盐酸和氢氧化钠充分反应;
③若出现气泡则说明可能是氢氧化钠变质,氢氧化钠溶液中含有碳酸钠;
④氢氧化钠若变质则产生碳酸钠,由于反应的情况不能确定,所以可以得出固体成分可能是碳酸钠,碳酸钠和氢氧化钠等猜想;
(4)设固体样品中碳酸钠的质量为x,跟碳酸钠反应的盐酸的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y×10% 2.2g
$\frac{106}{x}$=$\frac{73}{y×10%}$=$\frac{44}{2.2g}$
x=5.3g
y=36.5g
NaOH的质量为:13.3g-5.3g=8g
设和氢氧化钠反应的盐酸的质量为z
NaOH+HCl═NaCl+H2O
40 36.5
8g z×10%
$\frac{40}{8g}$=$\frac{36.5}{z×10%}$
z=73g
(3)在图中画出以纵坐标表示二氧化碳质量,横坐标表示盐酸的质量的关系图: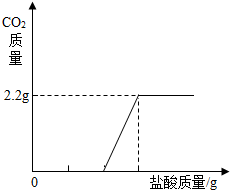 .
.
故答案为:方案一:(1)将pH试纸放在表面皿上,用玻璃棒蘸取少量待测液滴在试纸上,将试纸颜色与比色卡对照读出pH值;
(2)盐酸过量,溶液呈酸性,溶液的pH小于7;
方案二:(1)除去氧气和隔绝氧气;
(2)碱;
(3)取上述溶液加水稀释后,再滴加无色酚酞;溶液呈红色不消失;
方案三:(1)7;
(2)U型管中液面左低右高;
(3)①防止稀盐酸过量;
②使反应充分;
③氢氧化钠溶液中含有碳酸钠;
④Na2CO3,NaOH与Na2CO3的混合物;
(4)(1)样品中氢氧化钠的质量为8g;
(2)和氢氧化钠反应的盐酸的质量为73g;
(3) .
.
点评 本题主要考查了酸碱中和反应以及酸碱性溶液与酸碱指示剂相互作用的情况,可以依据已有的知识进行,要求同学们加强对物质性质的识记,以便灵活应用.


 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
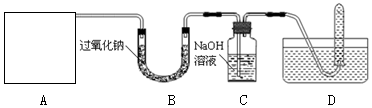
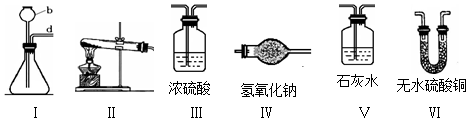
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
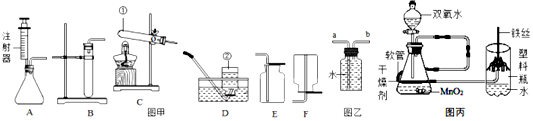
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素是一种有机物 | |
| B. | 在一个青蒿素分子中,C、H、O三种元素的原子个数比是15:22:5 | |
| C. | 青蒿素不属于氧化物 | |
| D. | 青蒿素分子中氧元素的化合价为-2价,则在生成该分子时,氧元素失去了两个电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3 纯碱 碱 | B. | CaO 生石灰 氧化物 | ||
| C. | O2 臭氧 单质 | D. | NaHCO3 苏打 盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com