
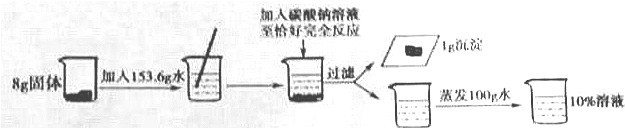
分析 (1)该实验氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,根据质量守恒定律正确书写化学方程式;
(2)根据化学方程式中各物质的质量比分析解答;
(3)根据化学方程式,结合沉淀的质量来计算出氢氧化钙的质量即可解答;
(4)随着反应的进行,氢氧化钙的质量逐渐减少,氢氧化钠的质量逐渐增大;
(5)根据化学方程式,结合沉淀的质量来计算出消耗碳酸钠的质量即可解答;
解答 解:(1)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(2)设消耗氢氧化钙的质量为x.
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
74 100
x 1g
则$\frac{74}{100}=\frac{x}{1g}$,
(3)设消耗氢氧化钙的质量为x.
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
74 100
x 1g
则$\frac{74}{100}=\frac{x}{1g}$,解得x=0.74g,则氢氧化钙和氢氧化钠混合物中氢氧化钠的质量为8g-0.74g=7.26g
故混合物中氢氧化钙和氢氧化钠质量的最简整数比:0.74g:7.26g=37:363;
(4)在滴加碳酸钠溶液的过程中,烧杯中溶质随着反应的进行,氢氧化钙的质量逐渐减少,氢氧化钠的质量逐渐增大;
(5)设消耗氢氧化钙的质量为x.
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
106 100 80
z 1g y
则$\frac{100}{80}=\frac{1g}{y}$,$\frac{106}{100}=\frac{z}{1g}$,解得y=0.8g,z=1.06g
所得溶液质量为:$\frac{7.26g+0.8g}{10%}$=80.6g;
所用Na2CO3溶液的质量为80.6g-(8g+153.6g-100g-1g)=20g
所用Na2CO3溶液中溶质质量分数为:$\frac{1.06g}{20g}$×100%=5.3%;
故答案为:
(1)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;(2)$\frac{74}{100}=\frac{x}{1g}$;(3)37:363;
(4)随着反应的进行,氢氧化钙的质量逐渐减少,氢氧化钠的质量逐渐增大;(5)5.3%.
点评 本题考查了氯化钠与碳酸钠的化学性质,同时考查了化学方程式的书写以及根据化学方程式计算溶液的质量分数,要求学生熟练掌握常见物质的化学性质以及相关的化学方程式.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:选择题
| A.物质区别 | B.灭火方法 |
| 区分食盐水和蛋白质溶液--用饱和 (NH4)2SO4溶液 | 电器着火--切断电源,用液态二氧化碳灭火器灭火 |
| C.实验记录 | D.生活常识 |
| 用10ml量筒量取7.25mL水 | 用洗涤剂洗油污--乳化作用 |
| A. | 物质区别 | B. | 灭火方法 | C. | 实验记录 | D. | 生活常识 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油锅着火用水浇 | |
| B. | 电器着火应先切断电源,再用二氧化碳灭火器扑灭 | |
| C. | 厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| D. | 扑灭森林火灾的有效方法之一是将大火蔓延路线前的一片树木砍掉 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
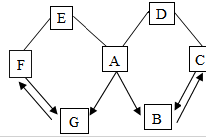 如图所示,A-G是初中化学常见的物质,其中B、C、D、E、F都是氧化物,图中“→”表示转化关系.“-”表示相互能反应,已知A是人体胃液中含有的酸,G是最轻的气体,B能作气体肥料,E是某些食品干燥剂的主要成分,D与A反应会生成黄色溶液,请回答:
如图所示,A-G是初中化学常见的物质,其中B、C、D、E、F都是氧化物,图中“→”表示转化关系.“-”表示相互能反应,已知A是人体胃液中含有的酸,G是最轻的气体,B能作气体肥料,E是某些食品干燥剂的主要成分,D与A反应会生成黄色溶液,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com