
分析 根据物质的性质进行分析,酸碱盐的溶液间两两混合,若能生成气体、沉淀或水,则反应能够进行,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:根据反应规律,金属和酸、金属和盐可发生置换反应,在金属活动性顺序中,铁在氢的前面,能与盐酸发生置换反应,铁与稀盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl2+H2↑;
铁在铜的前面,能与氯化铜溶液发生置换反应;铁与氯化铜溶液反应生成氯化亚铁和铜,反应的化学方程式为:Fe+CuCl2═FeCl2+Cu;故两个是置换反应;
氢氧化钠溶液与氯化铜溶液混合能产生氢氧化铜沉淀,化学方程式为CuCl2+Ca(OH)2=Cu(OH)2↓+CaCl2;碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;氢氧化钠溶液和盐酸发生中和反应生成氯化钠和水,化学方程式为反应的化学方程式为:HCl+NaOH=NaCl+H2O;氧化铁和盐酸反应生成氯化铁和水,化学方程式为Fe2O3+6HCl═2FeCl3+3H2O;氯化铜和碳酸钠反应生成碳酸铜沉淀和氯化钠,化学方程式为Na2CO3+CuCl2=CuCO3↓+2NaCl.符合复分解反应发生的条件,反应可以发生;故能发生的复分解反应共有5个.
故答案为:7;2;5;Fe+2HCl=FeCl2+H2↑;Fe+CuCl2═FeCl2+Cu;CuCl2+Ca(OH)2=Cu(OH)2↓+CaCl2;Na2CO3+2HCl═2NaCl+H2O+CO2↑;HCl+NaOH=NaCl+H2O;Fe2O3+6HCl═2FeCl3+3H2O;Na2CO3+CuCl2=CuCO3↓+2NaCl.
点评 本题考查了物质间的反应,完成此题,可以依据物质的性质结合复分解反应的条件进行.要求同学们熟记物质的性质以及有关物质的溶解性,以便灵活应用.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水(H2O)和过氧化氢(H2O2)分子中都含有氢元素 | |
| B. | 电解水实验证明水是由氢、氧两种元素组成的 | |
| C. | 用肥皂水可以区分软水和硬水 | |
| D. | 常用吸附、沉淀、过滤和蒸馏等方法净化水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
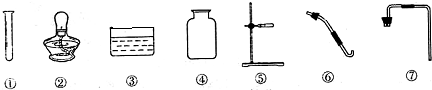
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com