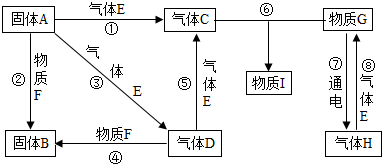
解:(1)由分析可知,反应物、生成物、反应条件,故化学方程式为C+O
2
CO
2;
(2)由分析可知,反应物、生成物,故化学方程式为Fe
2O
3+6HCl═2FeCl
3+3H
2O;
(3)由分析可知,反应物、生成物,故化学方程式为CuSO
4+2NaOH═Cu(OH)
2↓+Na
2SO
4;
(4)先明确置换反应的特点“单质+化合物=单质+化合物”,由分析可知,反应物、生成物、反应条件,故化学方程式为Fe+2HCl═FeCl
2+H
2↑或Fe+CuSO
4═FeSO
4+Cu或其他合理化学方程式;
(5)先明确分解反应的特点“一变多”,由分析可知,反应物、生成物、反应条件,故化学方程式为H
2CO
3═H
2O+CO
2↑或CaCO
3
CaO+CO
2↑或其他合理化学方程式.
故答为:(1)C+O
2
CO
2;
(2)Fe
2O
3+6HCl═2FeCl
3+3H
2O;
(3)CuSO
4+2NaOH═Cu(OH)
2↓+Na
2SO
4(4)Fe+2HCl═FeCl
2+H
2↑或Fe+CuSO
4═FeSO
4+Cu或其他合理化学方程式
(5)H
2CO
3═H
2O+CO
2↑或CaCO
3
CaO+CO
2↑或其他合理化学方程式
分析:(1)木炭在空气不充足条件下燃烧:可知反应物为木炭和氧气,生成物为二氧化碳,反应条件为点燃,故可书写化学方程式;
(2)用稀盐酸除去铁件表面的铁锈:可知反应物为稀盐酸和铁锈的主要成分氧化铁,生成物为氯化铁和水,故可书写化学方程式;
(3)向硫酸铜溶液中加入氢氧化钠溶液:可知反应物为硫酸铜溶液和氢氧化钠溶液,属于复分解反应的特点,则生成物为氢氧化铜沉淀和硫酸钠,故可书写化学方程式;
(4)有金属铁参加的置换反应:先明确置换反应的特点“单质+化合物=单质+化合物”,如铁与稀盐酸的反应,可知反应物为稀盐酸和铁,生成物为氯化亚铁和水,故可书写化学方程式;
(5)有CO
2气体生成的分解反应:先明确分解反应的特点“一变多”,如碳酸分解的化学方程式,可知反应物为碳酸,生成物为二氧化碳和水,故可书写化学方程式.
点评:确定反应物、生成物、反应条件,正确书写化学方程式;并且掌握书写化学方程式的方法和步骤;掌握确定反应类型的方法;掌握金属的化学性质.

 CO2;
CO2; CaO+CO2↑或其他合理化学方程式.
CaO+CO2↑或其他合理化学方程式. CO2;
CO2; CaO+CO2↑或其他合理化学方程式
CaO+CO2↑或其他合理化学方程式

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案