
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
| A、该反应的反应物为A和C |
| B、容器中发生的化学反应,属于化合反应 |
| C、反应后,待测A的质量为26g |
| D、化学反应中A与B质量比26:9 |


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、Ba(NO3)2、Na2CO3 |
| B、BaCl2、H2SO4 |
| C、KNO3、AgNO3 |
| D、FeCl3、NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验一 | 实验二 | 实验三 | |
| 实验方案 | 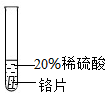 | 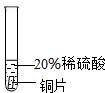 | 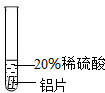 |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变为 | 铝片表面产生气泡较快 | |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢 | 铜不与稀硫酸反应 | |
| 三种金属在金属活动性顺序中的相应关系是 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com