(2010?南通)我国采用食盐中加入碘酸钾的方法防止缺碘引起的疾病.
(1)在人体中,碘是属于______(选填“常量”或“微量”)元素.
(2)碘酸钾(KIO3)中钾、碘、氧三种元素质量比为______;它受热易分解,烹饪时,添加加碘食盐应注意______.
(3)我国规定加碘食盐含碘量为20mg/kg~50mg/kg.为测定某加碘食盐是否为合格产品.在酸性条件下用足量KI溶液将其中KIO3全部转化成I2.反应方程式为:KIO3+5KI+6HCl=6KCl+3I2+3H2O.称取1000g某品牌加碘盐样品进行测定,经测定反应获得的I2的质量为152.4mg,试通过计算说明该加碘食盐是否为合格产品(计算过程写在答题纸上).
【答案】
分析:(1)根据生活常识及微量元素的有关知识解答.
(2)根据化学式的意义来求质量比;根据题干信息“它受热易分解”来分析.
(3)根据碘酸钾与碘化钾反应的化学方程式和生成碘单质的质量,列出比例式,即可计算出1000克食盐中含碘酸钾的质量,再由碘酸钾中碘元素的质量分数求出碘元素的质量,对照已知条件,即可知道样品是否符合国家标准.
解答:解:(1)碘属于微量元素.
(2)由碘酸钾的化学式KIO
3可知,碘酸钾由K、I、O三种元素组成,其分子含1个K原子、1个I原子和3个O原子;
根据碘酸钾的化学式可知KIO
3中钾元素、碘元素、氧元素的质量比=39:127:(16×3)=39:127:48;
由题意信息碘酸钾受热易分解,所以做饭时要等饭快熟时再加盐.
(3)根据碘酸钾与碘化钾反应的化学方程式和生成碘单质的质量,列出比例式,即可计算出1000克食盐中含碘酸钾的质量,再由碘酸钾中碘元素的质量分数求出碘元素的质量,对照已知条件,即可知道样品是否符合国家标准.
故答案为:
(1)微量 (2)39:127:48;不宜过早
(3)设KIO
3的质量为x
KIO
3 +5KI+6HCl=6KCl+3I
2+3H
2O
214 762
x 152.4mg
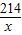
=
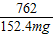
解之得 x=42.8mg
1000g加碘盐中的碘元素质量为42.8mg×
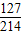
=25.4mg,
因为20mg/kg<25.4mg/kg<50mg/kg,
所以该加碘盐合格.
点评:本题主要考查了学生化学式的意义及利用化学方程式进行有关计算的能力.

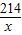 =
=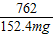
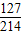 =25.4mg,
=25.4mg,