
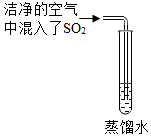
 雨、雪在形成和降落过程中吸收、溶解了空气中SO2、及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:
雨、雪在形成和降落过程中吸收、溶解了空气中SO2、及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:分析 (1)依据酸雨是pH小于5.6的降水可知要想证明是否是酸雨则要测定溶液的pH,据此分析即可.
(2)依据题干信息结合设计的实验可知,只要是证明亚硫酸的溶液pH能小于5.6即可完成相关的验证.
(3)依据对实验过程的叙述结合酸雨的成分和物之间的反应规律进行判断即可;
解答 解:(1)因为酸雨是pH小于5.6的降水,所以要想证明是否是酸雨则要测定溶液的pH.
A、蓝色石蕊试纸是检验溶液酸性时常用的试纸,不能准确测量溶液酸碱度;
B、紫色石蕊溶液只能检验溶液的酸碱性,不能检测溶液的酸碱度;
C、无色酚酞试剂只能检验溶液的酸碱性,不能检测溶液的酸碱度
D、pH试纸能较准确地测量溶液的酸碱强弱的程度,所以检验某地是否下酸雨可利用pH试纸进行测量;
(2)二氧化硫溶于水会生成亚硫酸,二氧化碳溶于水会生成碳酸,而CO2的饱和溶液常温下pH不小于 5.6,所以要想证明二氧化硫是形成酸雨的主要成分,只要证明实验中亚硫酸的溶液pH能小于5.6即可.
(3)某同学向一酸雨样品中滴加 CaCl2,溶液未观察到有浑浊现象,说明没有发生A反应,因为A反应进行时会有白色沉淀产生,能溶于HCl,所以两者也不可能同时生成,由于二氧化硫和二氧化碳性质相似,所以B反应能够发生,继续滴入NaOH溶液后即有白色沉淀产生,说明发生了C反应,同时溶液中含有的亚硫酸也可与氢氧化钠发生中和反应,所以D反应可能发生;
故答案为:(1)D;(2)H2SO3溶液的pH;溶液pH小于5.6;(3)A;
点评 此题是一道与酸雨相关的考查题,涉及到酸雨的形成及实验验证,借助题干信息结合相关的所学知识是解题的关键所在;


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.科学单位 | (1)能量和功率的单位都是J (2)Pa是压强的单位 (3)电流的单位是A (4)电压的单位是V |
| B.仪器原理 | (1)天平:等比杠杆 (2)弹簧测力计:弹簧的长度和拉力成正比 (3)液体温度计:液体的热胀冷缩 (4)密度计:漂浮 浮力等于重力 |
| C.符号意义 | (1)2O2:两个氧分子 (2)2H:两个氢原子 (3)$\stackrel{+1}{Na}$:正一价的钠元素 (4)Fe2+:铁离子 |
| D.能量转化 | (1)松开旋紧发条的八音盒,里面的圆盘旋转:弹性势能转化为动能 (2)核电站:核能转化为热能,再转化机械能,最后转化为电能 (3)电动机:电能转化为机械能 (4)电灯:电能转化为光能和热能 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液一定呈酸性 | B. | 溶液中肯定不含氢氧化钙 | ||
| C. | 溶液中不含氯化钙 | D. | 一定不含有盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤液中一定没有CuSO4,滤渣中一定有Cu | |
| B. | 滤液中一定没有H2SO4,滤渣中一定没有Fe | |
| C. | 滤液中可能含有CuSO4,滤渣中可能含有Fe | |
| D. | 滤液中一定含有FeSO4,可能含有CuSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com