
分析 赤铁矿的主要成分是氧化铁,高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
生石灰是氧化钙的俗称,能和水反应生成氢氧化钙,碳酸放出大量的热;
氨水和稀硫酸反应生成硫酸铵和水;
锌和硫酸铜反应生成硫酸锌和铜;
酒精燃烧生成水和二氧化碳.
解答 解:(1)赤铁矿炼铁过程中发生反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,反应前后气体的化学计量数之比是1:1.
故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;1:1.
(2)生石灰作为干燥剂的原理是:CaO+H2O═Ca(OH)2,该反应属于放热反应.
故填:CaO+H2O═Ca(OH)2;放.
(3)氨水与硫酸反应的化学方程式为:2NH3•H2O+H2SO4═(NH4)2SO4+2H2O,属于复分解反应.
故填:2NH3•H2O+H2SO4═(NH4)2SO4+2H2O;复分解.
(4)发生的反应是锌和硫酸铜反应,反应的化学方程式为:Zn+CuSO4═ZnSO4+Cu,连接电流表正极的是铜片.
故填:Zn+CuSO4═ZnSO4+Cu;铜.
(5)酒精(C2H6O)完全燃烧的化学方程式为:C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
酒精的某种水溶液中溶质和溶剂的氢原子个数相等,则该溶液中溶质的质量分数为:$\frac{46}{46+54}$×100%=46%.
故填:C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;46%.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.| 操作方法 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,向其中滴加足量的稀盐酸 ②取少量滤液于试管中,向其中加入碳酸钠溶液 ③取两只试管,分别加入少量的滤液,分别滴加足量的稀盐酸和碳酸钠溶液 | 有气泡产生 有沉淀产生 以上两只试管均无现象 | 则C中的废液成分是NaOH、NaCl、Na2CO3 则C中的废液成分是NaOH、NaCl、Ca(OH)2 则C中的废液成分是NaOH、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 反应前 | 反应后 |  | ||
| 甲 | 乙 | 丙 | 丁 | |
 |  |  |  | |
| A. | 图中有四种不同的氧化物 | B. | 反应前后分子总数不变 | ||
| C. | 反应前后各元素化合价不变 | D. | 生成物中丙和丁的质量比为22:7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
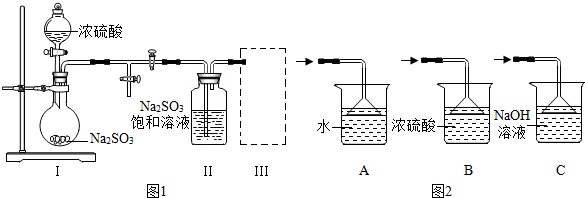
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
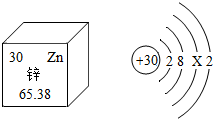
| A. | 单质 | B. | 化合物 | C. | 元素 | D. | 原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 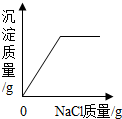 在一定量的AgNO3溶液中逐滴加入NaCl溶液 在一定量的AgNO3溶液中逐滴加入NaCl溶液 | |
| B. | 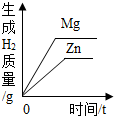 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 | |
| C. |  向NaOH溶液中逐滴加入稀盐酸 向NaOH溶液中逐滴加入稀盐酸 | |
| D. |  向NaOH和Na2CO3的混合溶液中,逐滴加入稀盐酸 向NaOH和Na2CO3的混合溶液中,逐滴加入稀盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 江西不仅山清水秀、景色迷人,特色美食更是遍布各地令各路“吃货”流连忘返.
江西不仅山清水秀、景色迷人,特色美食更是遍布各地令各路“吃货”流连忘返.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com