
如图所示是初中常见化学物质间的转化关系(部分生成物及反应条件已略去),其中A~E均为氧化物,且A、C组成元素相同,E中两种元素的质量比为7:3,甲、乙、丙、丁均为单质。请回答下列问题:
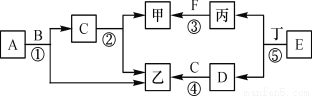
(1)F的化学式可能是 。
(2)反应①中B物质的作用是 。
(3) 反应①~⑤中属于置换反应的是 。
(4)反应⑤的化学方程式 。
(1)HCl(或H2SO4) (2)催化作用 (3)③⑤(4)3C+2Fe2O34Fe+3CO2↑ 【解析】 试题分析:A、C组成元素相同,且都是氧化物,说明A是过氧化氢和C是水,乙是氧气,水会发生电解产生氢气和氧气,所以甲是氢气,丙能够获得氢气,说明丙是金属,所以⑤是冶炼金属的过程,E中两种元素的质量比为7:3,根据计算确定E是氧化铁,所以D是二氧化碳,而二氧化碳会经过光合作用...科目:初中化学 来源:福建省洛江区2018届初三化学模拟考试试卷 题型:单选题
古语道:“人要实,火要虚”.此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺.从燃烧的条件看,“火要虚”的实质是
A. 增大可燃物的热值 B. 提高空气中氧气的含量
C. 提高可燃物的着火点 D. 增大可燃物与空气的接触面积
D 【解析】试题分析:充分燃烧需要充足的氧气和足够大的接触面。火要虚是指增大接触面,因此选D。查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2018届九年级5月一模化学试卷 题型:科学探究题
某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
【提出问题】①三种溶液的酸碱性?
②它们与酸反应时溶液的pH如何变化?
【查阅资料】
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
【实验1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
【实验2】向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。

【实验3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。

【解释与结论】
(1)实验1得出三种溶液的碱性由强到弱的顺序为________________。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是_________,实验结束,向反应后的溶液中滴加紫甘蓝汁液,观察到的现象是_________。
(3)实验3中,b点的溶质为_________,c点后发生反应的化学方程式为_________。
(4)依据实验3获取的信息,鉴别Na2CO3和NaHCO3固体的实验方案为_________。
氢氧化钠溶液>碳酸钠溶液>碳酸氢钠溶液 实验过程中溶液的pH由大于7到小于7,说明氢氧化钠被消耗 溶液变为紫红色 NaCl、HCl NaHCO3+ HCl=NaCl+ H2O+CO2↑ 取两种固体加水配成溶液,分别逐滴加入盐酸,若立即产生气泡则为碳酸氢钠,若开始无气泡,一段时间后有气泡,则为碳酸钠。 【解析】(1)碳酸氢钠溶液使紫甘蓝汁液变蓝,其PH在8~9间,碳酸钠溶液使紫甘蓝汁液变绿,其...查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2018届九年级5月一模化学试卷 题型:单选题
某纯净物X燃烧的化学方程式为X+3O2 点燃 2CO2+2H2O,则X的化学式为
A. C2H2 B. C2H4 C. C2H6O D. C2H6
B 【解析】由质量守恒定律:反应前后,原子种类、数目均不变,X+3O22CO2+2H2O,反应前碳、氢、氧原子个数分别为0、0、6,反应后的生成物中碳、氢、氧原子个数分别为2、4、6,根据反应前后原子种类、数目不变,则每个X分子由2个碳原子和4个氢原子构成,则物质X的化学式为C2H4。故选D。查看答案和解析>>
科目:初中化学 来源:山东省烟台龙口市2018届九年级下学期期中考试化学试卷 题型:科学探究题
某研究性学习小组通过查阅资料获知以下信息:将二氧化碳气体慢 慢地通入一定量的氢氧化钠溶液中,在溶液中先后发生以下两个化学反应:
2NaOH +CO2=Na2CO3+H2O (先发生反应) Na2CO3+CO2+H2O=2NaHCO3(后发生反应)
同学们开展了下列探究活动:
【提出问题】 将二氧化碳气体慢慢地通入一定量的氢氧化钠溶液中, 反应后所得溶液中溶质的成分有哪些?
【猜想假设】Ⅰ.NaHCO3 和 Na2CO3; Ⅱ.只有 NaHCO3 ;
Ⅲ.__________________ ; Ⅳ._____________________ .
小资料:Na2CO3+HCl=NaHCO3+NaCl NaHCO3+HCl= NaCl+H2O+CO 2↑
NaHCO3+NaOH=Na2CO3+H2O
【实验探究】 学习小组的同学将二氧化碳气体慢慢地通入一定量的某氢氧化钠溶液中,对溶液的成分进行探究后发现猜想Ⅲ、Ⅳ是不成立的。
为了进一步验证剩下的猜想,按下列流程进行实验并测出相关数据:

【获得结论】 根据上述信息, 分析反应后所得溶液中溶质的成分为__________,X溶液为____________,所得溶液A的成分为 _____________________
NaOH和 Na2CO3 Na2CO3 NaHCO3 和 Na2CO3 NaOH溶液 NaOH和Na2CO3 【解析】【猜想假设】如果氢氧化钠过量,则溶液中的溶质是没参与反应的NaOH和生成的Na2CO3,如果恰好反应,溶质是Na2CO3【实验探究】因为NaHCO3+NaOH=Na2CO3+H2O,所以加入的过量X溶液是NaOH溶液,BaCl2 + Na2CO3 == BaCO3↓+ 2Na...查看答案和解析>>
科目:初中化学 来源:山东省烟台龙口市2018届九年级下学期期中考试化学试卷 题型:多选题
下列各组稀溶液中,不用其他试剂不能鉴别出来的是
A. Na2CO3、H2SO4、HCl、NaNO3 B. HCl、K2CO3、BaCl2、Na2SO4
C. CuSO4、NaOH、KNO3 、KOH D. NaOH、NaCl、HCl、FeCl3
AC 【解析】A. Na2CO3、H2SO4、HCl、NaNO3 ,盐酸有刺激性气味,与碳酸钠反应生成气体,碳酸钠与硫酸反应生成气体。 B. HCl、K2CO3、BaCl2、Na2SO4,盐酸有刺激性气味,与碳酸钾反应生成气体,碳酸钾与氯化钡反应生成白色沉淀。C. CuSO4、NaOH、KNO3 、KOH,硫酸铜蓝色溶液,与氢氧化钠,氢氧化钾均生成蓝色沉淀。D. NaOH、NaCl、HCl、...查看答案和解析>>
科目:初中化学 来源:山东省烟台龙口市2018届九年级下学期期中考试化学试卷 题型:单选题
下列是分析久置于空气中的NaOH固体的相关实验(不考虑水分),其中合理的是( )
序号 | 实验目的 | 实验方案 |
① | 证明变质 | 取少量固体,加水溶解,滴加足量稀盐酸,观察是否有气泡产生 |
② | 确定成分 | 取少量固体,加入石灰水,过滤,向滤液中滴加酚酞试液 |
③ | 测定纯度 | 取a g样品与足量氯化钡溶液充分反应,将沉淀过滤、洗涤、干燥,得到mg固体 |
④ | 除去杂质 | 取固体,加水溶解,滴加氯化钙溶液至恰好完全反应,过滤 |
A. ①② B. ①③ C. ②④ D. ③④
B 【解析】试题分析:①氢氧化钠变质后可形成碳酸钠,在滴加盐酸时碳酸钠可与盐酸反应生成二氧化碳气体;如不产生气体则碳酸钠不存在,即氢氧化钠未变质。此项正确。②加入的石灰水呈碱性(或与碳酸钠反应生成氢氧化钠),所以无法再通过加酚酞确定氢氧化钠是否存在。此项不正确。③生成的沉淀为碳酸钠与氯化钡反应生成的碳酸钡;可根据其质量计量出碳酸钠的质量,并进一步完成纯度计算。此项正确。④如加入氯化钙,则可与...查看答案和解析>>
科目:初中化学 来源:天津市河北区2018届九年级会考化学试卷 题型:单选题
已知碳酸镁在空气中煅烧可生成氧化镁和二氧化碳。现有镁粉和碳酸镁混合物,将该混合物充分煅烧。若煅烧前后固体质量不变,则原混合物中镁粉所占的质量分数为
A. 22% B. 44%
C. 66% D. 88%
B 【解析】【解析】 设原混合物中镁的质量为x,碳酸镁的质量为y, ①2Mg+O22MgO,②MgCO3MgO+CO2↑, 48 80 84 40 x y 反应①中剩余固体质量为:,反应②中剩余固体质量为:, 根据题意得:+=x+y,解得:x:y=11:14, 则原混合物中镁粉的质量分数为:×100%=44%。故选B。查看答案和解析>>
科目:初中化学 来源:云南民族大学附属中学2018届九年级下学期第二次月考化学试卷 题型:单选题
 常用于在接触法制硫酸过程中产生
常用于在接触法制硫酸过程中产生 ,其化学方程式为:4FeS2 +11O2
,其化学方程式为:4FeS2 +11O2  2X+8SO2,则X的化学式为
2X+8SO2,则X的化学式为
A. FeO B.  C.
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com