
 ĀČ»ÆÄĘŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬µē½āĀČ»ÆÄĘČÜŅŗæÉÖʵĆĀČĘų”¢ĒāŃõ»ÆÄʵČĪļÖŹ£¬·¢ÉśµÄ»Æѧ·“Ó¦ČēĻĀ£ŗ2NaCl+2H2O $\frac{\underline{\;Ķصē\;}}{\;}$Cl2”ü+H2”ü+2NaOH ĻÖČ”Ņ»¶ØÖŹĮæµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĀČ»ÆÄĘČÜŅŗ½ųŠŠµē½ā£¬µ±ĀČ»ÆÄĘĶźČ«·“Ó¦Ź±£¬Ķ£Ö¹Ķصē£®Éś³ÉĀČĘųµÄÖŹĮæÓė·“Ó¦Ź±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė¼ĘĖć£ŗ
ĀČ»ÆÄĘŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬µē½āĀČ»ÆÄĘČÜŅŗæÉÖʵĆĀČĘų”¢ĒāŃõ»ÆÄʵČĪļÖŹ£¬·¢ÉśµÄ»Æѧ·“Ó¦ČēĻĀ£ŗ2NaCl+2H2O $\frac{\underline{\;Ķصē\;}}{\;}$Cl2”ü+H2”ü+2NaOH ĻÖČ”Ņ»¶ØÖŹĮæµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĀČ»ÆÄĘČÜŅŗ½ųŠŠµē½ā£¬µ±ĀČ»ÆÄĘĶźČ«·“Ó¦Ź±£¬Ķ£Ö¹Ķصē£®Éś³ÉĀČĘųµÄÖŹĮæÓė·“Ó¦Ź±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė¼ĘĖć£ŗ·ÖĪö øł¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½¼°ĘäĢį¹©µÄŹż¾ŻæÉŅŌ½ųŠŠĻą¹Ų·½ĆęµÄ¼ĘĖćŗĶÅŠ¶Ļ£®
½ā“š ½ā£ŗ£Ø1£©ÉčĀČ»ÆÄĘÖŹĮæĪŖx£¬Éś³ÉĒāĘųÖŹĮæĪŖy£¬Éś³ÉĒāŃõ»ÆÄĘÖŹĮæĪŖz£¬
2NaCl+2H2O $\frac{\underline{\;Ķصē\;}}{\;}$ Cl2”ü+H2”ü+2NaOH£¬
117 71 2 80
x 7.1g y z
$\frac{117}{x}=\frac{71}{7.1g}=\frac{2}{y}=\frac{80}{z}$
x=11.7g£¬y=0.2g£¬z=8g£¬
£Ø2£©²Ī¼Ó·“Ó¦µÄ10%µÄĀČ»ÆÄĘČÜŅŗÖŹĮæĪŖ£ŗ11.7g”Ā10%=117g£¬
£Ø3£©·“Ó¦ŗóĖłµĆČÜŅŗÖŠČÜÖŹÖŹĮæ·ÖŹżĪŖ£ŗ$\frac{8g}{117g-7.1g-0.2g}$”Į100%=7.293%£¬
“š£ŗ£Ø1£©·“Ӧɜ³ÉH2µÄÖŹĮæŹĒ0.2g£®
£Ø2£©²Ī¼Ó·“Ó¦µÄ10%µÄĀČ»ÆÄĘČÜŅŗÖŹĮæĪŖ117g£®
£Ø3£©·“Ó¦ŗóĖłµĆČÜŅŗÖŠČÜÖŹÖŹĮæ·ÖŹżĪŖ7.293%£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éѧɜŌĖÓĆ¼ŁÉč·ØŗĶ»Æѧ·½³ĢŹ½½ųŠŠ¼ĘĖćŗĶĶʶĻµÄÄÜĮ¦£¬¼ĘĖ揱ŅŖ×¢Ņā¹ę·¶ŠŌŗĶ×¼Č·ŠŌ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ū | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
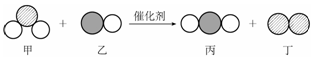
| A£® | ŅŅŗĶ±ūÖŠĖłŗ¬ŌŖĖŲÖÖĄąĻąĶ¬ | B£® | ¼×ŗĶ¶”ÖŠĶ¬ÖÖŌŖĖŲ»ÆŗĻ¼Ū²»ĻąµČ | ||
| C£® | øĆ·“Ó¦ÖŠ¹²ÓŠČżÖÖŌŖĖŲ | D£® | ±ūæÉÄÜŹĒ¶žŃõ»ÆĮņ·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²ŹĘģĘ®Ńļ | B£® | ĘųĒņÉżæÕ | C£® | ĄńÅŚŗäĆł | D£® | ÉłŅōŌ¶Ńļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
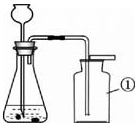 ČēĶ¼ĖłŹ¾ŹĒŹµŃéŹŅÖĘČ”ĘųĢåµÄ³£¼ū×°ÖĆ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼ĖłŹ¾ŹĒŹµŃéŹŅÖĘČ”ĘųĢåµÄ³£¼ū×°ÖĆ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | +1 | B£® | +2 | C£® | -l | D£® | -2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com