
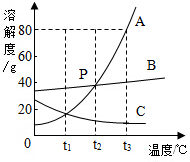
 如图是A、B、C三种固体物质的溶解度曲线,回答下列问题
如图是A、B、C三种固体物质的溶解度曲线,回答下列问题分析 (1)根据溶解度曲线交点的含义进行分析;
(2)据物质的溶解度曲线可比较同一温度下不同物质的溶解度大小;
(3)根据物质的溶解度曲线可以判断一定温度时,一定量的溶剂中能够溶解的溶质质量;
(4)从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶;
(5)根据t2℃、t1℃时三种物质的溶解度大小关系,三种物质溶解度受温度的影响的变化趋势判断降温后溶液是否析出晶体、是否饱和,进而确定所得溶液中溶质的质量分数的大小.
解答 解:(1)P点是t2℃时,A、B的溶解度曲线的交点,表示该温度下两物质的溶解度相等;
(2)t1℃时A、B、C三种物质的溶解度由大到小的顺序B>A=C;
(3)t3℃时A的溶解度是80g,即100g水中最多溶解80g的A,所以将40克A加到50克水中,充分搅拌后恰好溶解,得到溶液的质量为90g;
(4)A物质的溶解度受温度变化影响较大,因此要从A的热溶液中获得晶体,应采用最适宜的方法是冷却热饱和溶液或降温结晶;
(5)t2℃时,将A、B、C的饱和溶液(都含有100g水),降温到t1℃时A的溶解度变化最大,析出晶体最多,C溶解度减小,无晶体析出;
饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,即溶解度大则溶质的质量分数大,由于在t2℃时,三种物质的溶解度大小关系是A=B>C,即在t2℃时,三种物质的饱和溶液中溶质的质量分数:A=B>C;由于A和B的溶解度随温度的降低而减小,因此降温至t1℃时,A和B的溶液中都会有晶体析出,溶液都还是饱和溶液,由于在t1℃时三种物质的溶解度B>A=C,而由于C的溶解度随温度的降低而增大,因此降温至t1℃时,它的饱和溶液就会变成不饱和溶液,但由于溶液的组成没有发生改变,故C溶液中溶质的质量分数不变,与降温前相等,其溶解度小于t1℃,由图可知,C的溶液中溶质的质量分数还是最小;故所得溶液的溶质质量分数由小到大依次为CAB;
故答案为:(1)t2℃时,A、B的溶解度相等;
(2)B>A=C;
(3)90;
(4)冷却热饱和溶液(或降温结晶);
(5)A;C;CAB.
点评 本题难度不是很大,主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.


科目:初中化学 来源: 题型:解答题
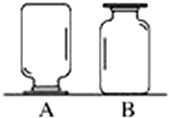 如图,在实验台上放置两瓶气体,集气瓶A、B中盛有二氧化碳(密度比空气的大)、氧气(密度比空气的大)、氢气(密度比空气的小)中的一种.小刚和小强想对瓶中气体进行探究:
如图,在实验台上放置两瓶气体,集气瓶A、B中盛有二氧化碳(密度比空气的大)、氧气(密度比空气的大)、氢气(密度比空气的小)中的一种.小刚和小强想对瓶中气体进行探究:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选 项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 氧化钙 | 石灰石 | 高温 |
| B | 稀盐酸 | 稀硝酸 | 加入过量的硝酸银溶液,过滤 |
| C | 氯化钠 | 泥沙 | 加入足量的水,溶解、蒸发、结晶 |
| D | 氯化镁溶液 | 稀盐酸 | 加入过量的氢氧化镁,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com