
| A. | 浓硫酸能电离出氢离子,但不具有酸的通性 | |
| B. | 将足量的Zn放入少量的浓硫酸中,反应后生成的气体只有SO2 | |
| C. | 在上述化学反应中,反应物之间电子发生了转移,属于氧化还原反应 | |
| D. | 在上述化学反应前后,溶液的质量相等,遵循质量守恒定律 |
分析 A、浓硫酸能电离出氢离子,具有酸的通性;
B、当锌与浓硫酸反应时,随着浓硫酸的不断消耗,浓硫酸逐渐变成稀硫酸,锌能与稀硫酸反应生成氢气;
C、有电子发生转移的反应,属于氧化还原反应;
D、上述化学反应前后,溶液的质量减少.
解答 解:A、浓硫酸能电离出氢离子,具有酸的通性,错误;
B、当锌与浓硫酸反应时,随着浓硫酸的不断消耗,浓硫酸逐渐变成稀硫酸,锌能与稀硫酸反应生成氢气,故反应后生成的气体有SO2和氢气,错误;
C、在上述化学反应中,反应物之间电子发生了转移,属于氧化还原反应,正确;
D、上述化学反应前后,溶液的质量减少,错误.
故选C.
点评 本题考查了金属的性质和酸的性质,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:选择题
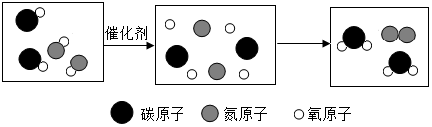
| A. | 反应前有两种物质的分子 | |
| B. | 化学变化的本质是:分子分成原子,原子重新组合成新物质的分子 | |
| C. | 在化学变化中,分子分成原子,原子重新组合成新物质 | |
| D. | 图中共有三种氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师指导下,将7克高锰酸钾充分加热,得到氧气600厘米3 | 解:高锰酸钾中氧元素的质量分数: =$\frac{O的相对原子质量×4}{KMn{O}_{4}的相对分子质量}$×100%=$\frac{16×4}{39+55+16×4}$×100%=40.5% 氧气的质量为7克×40.5%=2.84克 答:7克高锰酸钾完全分解产生氧气2.84克. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ZnSO4 NaNO3 KCl | B. | Cu(NO3)2 NaCl KNO3 | ||
| C. | Na2CO3 KNO3 NH4Cl | D. | K2SO4 Ba(OH)2 KCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 反应前 | 氧化铜完全反应后 | |
| Ⅰ组 | 洗气瓶和石灰水的质量为185g | 洗气瓶和瓶内物质的总质量为187g |
| Ⅱ组 | 玻璃管和氧化铜样品的质量为57.9g | 玻璃管和玻璃管内物质的质量为56.1g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com