
分析 (1)根据常见的化学仪器的名称,根据实验室中制取二氧化碳的反应原理、二氧化碳的检验方法,进行分析解答.
(2)根据湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,说明有酸性物质生成,进行分析解答.
(3)根据题意,当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,是因为二氧化碳与水、碳酸钠溶液反应生成碳酸氢钠,进行分析解答.
(4)根据题意,20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g.20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g,结合二氧化碳与氢氧化钠反应生成碳酸钠和水,进行分析解答.
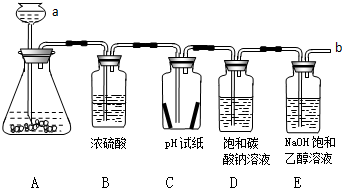
解答 解:(1)仪器a的名称是长颈漏斗;装置A中大理石或石灰石和稀盐酸反应来制取,属于固液常温型,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.二氧化碳不能燃烧、不能支持燃烧,在b处检验是否有CO2逸出的操作是收集二氧化碳验满的方法为将燃着的木条放在导管口,木条熄灭,说明有气体逸出.
(2)装置C中放有干和湿的pH试纸各一张,当通入CO2一段时间后,湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,是因为二氧化碳能与水反应生成碳酸,碳酸显酸性,说明了CO2与水反应后的溶液显酸性.
(3)当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,是因为二氧化碳与水、碳酸钠溶液反应生成碳酸氢钠,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3↓.
(4)20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g.20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g.当通入CO2一段时间后,二氧化碳与水反应生成碳酸钠和水,碳酸钠在乙醇中几乎不溶解,故装置E中观察到的实验现象是出现白色沉淀(或浑浊)反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
故答案为:(1)长颈漏斗;CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在导气管口,观察木条是否熄灭;
(2)CO2与水反应后的溶液显酸性;
(3)Na2CO3+CO2+H2O=2NaHCO3↓;
(4)出现白色沉淀(或浑浊);2NaOH+CO2=Na2CO3+H2O.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取二氧化碳气体的反应原理、二氧化碳的化学性质等是正确解答本题的关键.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
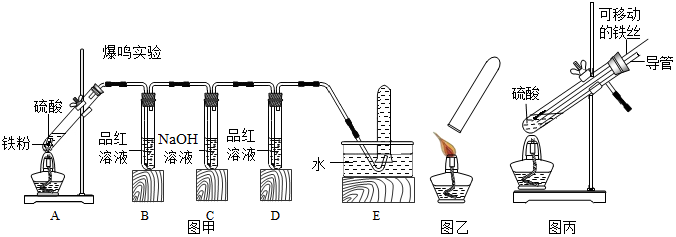
| A中硫酸的浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验三 | 25% | ③ | 不褪色 | ④ | 只有H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 学习化学一年后,同学们对课本上“支持燃烧的气体一般是氧气”这句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
学习化学一年后,同学们对课本上“支持燃烧的气体一般是氧气”这句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:| 实验操作 | 实验现象 | 实验结论 | |
| 方案1 | 取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察 | 溶液变成红色 | 白色物质中一定有氧化钠 |
| 方案2 | 取该样品少量于试管里,滴加足量盐酸,观察 | 溶液中有气泡冒出 | 白色物质中一定有碳酸钠. |
| 方案3 | (1)取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液溶液 (供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液) (2)过滤,再向滤液里滴加无色酚酞试液. | 出现白色沉淀 无明显现象出现 | 乙(在甲、乙、丙中选)的猜想成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲溶液呈中性,乙溶液呈碱性 | |
| B. | 甲溶液属于酸性溶液,乙溶液属于碱性溶液 | |
| C. | 甲溶液一定是酸性溶液,乙溶液一定是碱性溶液 | |
| D. | 甲溶液使无色酚酞变红色,乙溶液不能使无色酚酞变色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  某温度下,向一定量不饱和硝酸钾溶液中不断加入硝酸钾晶体 | |
| B. |  向一定量的稀盐酸中逐滴滴加水 | |
| C. |  向一定量的氢氧化钠和碳酸钠的混合溶液中逐滴滴加盐酸 | |
| D. |  向一定量氯化铜溶液中加入一定量铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com