
【题目】MnO2是一种重要的无机功能材料,粗MnO2(含有较多的MnO和MnCO3)的提纯是工业生产的重要环节.如图是某研究性学习小组在实验室中模拟工业上粗MnO2转化为MnO2的工艺流程. 
请回答下列问题:
(1)操作A的名称是 .
(2)NaClO3中氯元素的化合价为价.
(3)蒸发所需的仪器有铁架台(带铁圈)、蒸发皿、酒精灯和 .
(4)写出加稀硫酸H2SO4时产生CO2的化学方程式 .
(5)该流程中可以循环利用的物质是H2SO4和 .
【答案】
(1)过滤
(2)+5
(3)玻璃棒
(4)MnCO3+H2SO4═MnSO4+H2O+CO2↑
(5)NaClO3
【解析】解:(1)将溶液和固体分离的方法叫做过滤,故填过滤;(2)根据在化合物中元素化合价的代数和为零的原则,设氯元素的化合价为a,则+1+a+(﹣2)×3=0,a=+5;(3)蒸发时需要玻璃杯搅拌,使受热均匀,故还需要玻璃棒;(4)碳酸锰和硫酸反应生成硫酸锰、水和二氧化碳,反应的化学方程式为:MnCO3+H2SO4═MnSO4+H2O+CO2↑;(5)由工艺流程图可以看出,循环利用的是H2SO4和NaClO3;所以答案是:(1)过滤;(2)+5;(3)玻璃棒;(4)MnCO3+H2SO4═MnSO4+H2O+CO2↑;(5)NaClO3;
【考点精析】认真审题,首先需要了解过滤操作的注意事项(过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损),还要掌握蒸发操作的注意事项(蒸发注意点:1、在加热过程中,用玻璃棒不断搅拌2、当液体接近蒸干(或出现较多量固体)时停止加热,利用余热将剩余水分蒸发掉,以避免固体因受热而迸溅出来.3、热的蒸发皿要用坩埚钳夹取,热的蒸发皿如需立即放在实验台上,要垫上石棉网)的相关知识才是答题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究. [查阅资料]
名称 | 食用纯碱 | 食用小苏打 |
主要成分 | Na2CO3 | NaHCO3 |
酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
[实验探究]
(1)探究两者水溶液酸碱性的差异 小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变色,但食用纯碱溶液中颜色更深,由此推测可能溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用进行测定.
(2)验证两种粉末的稳定性 在老师的指导下,该小组按如图1装置进行实验操作,观察到(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为 , 装置中棉花的作用是 .
(3)测定食用纯碱粉末的纯度 取食用纯碱粉末试样,利用如图2装置进行实验测定.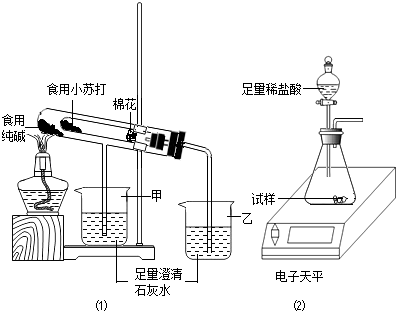
数据记录如下:
称量项目 | 称量时间 | 质量/g |
试样 | 11.0 | |
装置+稀盐酸 | 160.0 | |
装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
反应生成CO2的质量为g.
(4)通过计算确定食用纯碱粉末中Na2CO3的质量分数.(写出计算过程,结果保留一位小数.)
(5)如果测得的结果比实际纯度高,可能的原因是 . (答一种即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据要求填空:
(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝.金属大规模被使用的先后顺序跟(选填字母)(A.地壳中金属元素的含量 B.金属的导电性 C.金属的活动性)关系最大; 目前世界上已有50%以上的废钢铁得到回收利用,其目的是A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈;
生锈的铁制品放入盛有过量稀盐酸的洗槽中,观察到溶液变黄,有无色气泡逸出.写出其中一个反应的化学方程式 , 其反应类型是 . 若要验证银、铁、锌的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是、 .
(2)A、B两种固体物质溶解度曲线如图所示. ①t1℃时,A和B的溶解度大小关系是 .
②把t1时,A和B的饱和溶液变成不饱和溶液,除了升高温度外,还可以采取的方法有 .
③t2℃时,A的溶解度为25g,在t2℃时,向50g水中加入20g的A物质,充分溶解所得溶液的溶质质量分数为 .
④A中混有少量的杂质B,若想得到较为纯净的A,可以采用的方法是 . 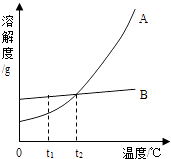
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用“一定”“不一定”填空.
(1)碱溶液的pH__________大于7;(2)酸溶液___________使石蕊试液变红; (3)使酚酞试液变红的溶液__________________是碱溶液.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式并填空.
(1)碳在过量氧气中充分燃烧:该反应属于(选填“放热”或“吸热”)反应.
(2)锌和稀硫酸反应:;反应类型是
(3)盐酸与碳酸氢氨反应:;明显的现象是
(4)实验室加热高锰酸钾制取氧气:在发生装置的试管口放一团棉花的作用是
(5)用熟石灰和硫酸铜溶液制备波尔多液:反应类型是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下列仪器制取相关气体,不能实现的是( ) 
A.用锌和稀硫酸制取氢气
B.用双氧水和二氧化锰制取氧气
C.用高锰酸钾加热分解制取氧气
D.用石灰石和稀盐酸制取二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
A | H2O | CO2 | CuO | O2 |
B | CuSO4 | H2SO4 | HCl | Fe |
C | NaCl | Na2CO3 | KNO3 | NaOH |
D | CaO | CaCO3 | Ca(OH)2 | H2O |
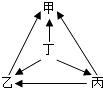
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组利用如图所示实验装置进行了以下探究实验.步骤如下: 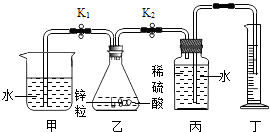
①检查装置气密性,加入锌粒和稀硫酸;
②关闭K2、打开K1 , 待气泡连续均匀产生,立即关闭K1、打开K2 , 并开始计时;
③待丁中收集到10mL水,结束计时;
④换不同溶质质量分数、不同体积的稀硫酸,与质量相同的同一种锌粒重复上述实验;
⑤将每次实验的数据记录于下表:
硫酸用量(mL) | 40 | 40 | 20 | 20 | 20 | 10 | 10 |
硫酸的溶质质量分数(%) | 9.8 | 39.2 | 9.8 | 19.6 | 39.2 | 19.6 | 39.2 |
收集所用时间 | 4′03 | 1′36 | 4′12 | 3′30 | 1′40 | 3′42 | 1′48 |
(1)写出乙中反应的化学方程式:;
(2)该实验的目的是:;
(3)上述实验证明:对该反应中氢气产生的速率有显著影响;
(4)若要快速制取大量氢气,可在乙中加入几滴硫酸铜溶液,但加入的量不可过多,原因是:(用化学方程式表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com