
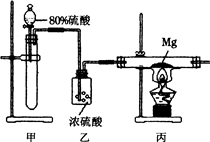
 已知SO2和CO2都是非金属氧化物,两者的实验室制法和化学性质都具有一定的相似性.但SO2比CO2易溶于水,与水反应生成H2SO3,H2SO3易与O2化合.
已知SO2和CO2都是非金属氧化物,两者的实验室制法和化学性质都具有一定的相似性.但SO2比CO2易溶于水,与水反应生成H2SO3,H2SO3易与O2化合. 2MgO+C.某研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验.
2MgO+C.某研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验. 2MgO+S;
2MgO+S; 2MgO+S;(3)有; SO2有毒,会污染大气 在装置丙后增添一个吸收SO2的装置.
2MgO+S;(3)有; SO2有毒,会污染大气 在装置丙后增添一个吸收SO2的装置.

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:天门 题型:问答题
| ||
查看答案和解析>>
科目:初中化学 来源:2009年湖北省仙桃市、天门市、潜江市、江汉油田中考化学试卷(解析版) 题型:填空题
 2MgO+C.某研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验.
2MgO+C.某研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验.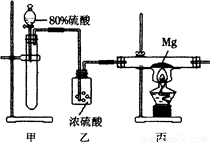
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com