
��֪����ˮ��Ӧ�Ļ�ѧ����ʽΪ��2Na+2H2O = 2NaOH + H2����������Ϊm g���ơ�þ��п���ֽ����ֱ���25 g ��������Ϊ19.6% ��ϡ���ᷴӦ��
���������ڽ���������ȷ����������������������С�ж��ֿ��ܣ�������þ��ˮ�ķ�Ӧ������þ��п����������������ͬ�Ҷ�С���Ʋ��������������������ʾΪNa>Mg��Zn ���밴���ϱ�ʾ��д�����п��������
______________________________________________________________________________��
��������ȷ������������������������СΪNa>Mg��Znʱ��m��ȡֵ��Χ________________��
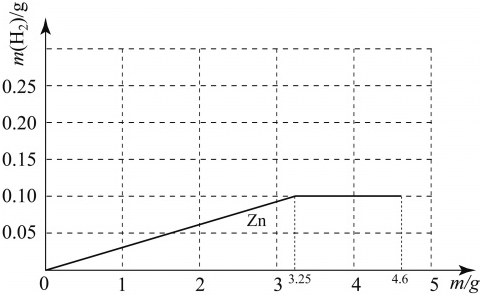
������m�� 4.6 ʱ��Zn���ᷴӦ����H2�����������������m���Ĺ�ϵ����ͼ������ͼ���ٻ����ƺ�þ���ֽ����ֱ����ᷴӦ����H2�����������������m���Ĺ�ϵͼ�ߡ�����ͼ������Ԫ�ط���ע����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
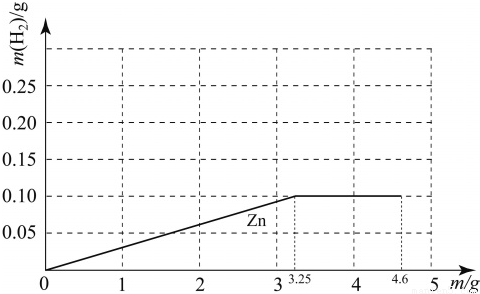
��Ŀ�����л�ѧ ��Դ��2010��ڶ�ʮ�조��ԭ����ȫ������ѧ����ѧ���ʺ�ʵ���������������Ծ��������棩 ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�����ţ����꼶��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪����ˮ��Ӧ�Ļ�ѧ����ʽΪ��2Na+2H2O= 2NaOH+ H2����������Ϊm g���ơ�þ��п���ֽ����ֱ���25 g��������Ϊ19.6% ��ϡ���ᷴӦ�����ڽ�����������ȷ����������������������С�ж��ֿ��ܣ�������þ��ˮ�ķ�Ӧ������þ��п����������������ͬ�Ҷ������Ʋ��������������������ʾΪMg��Zn >Na����m=3gʱ�����б�ʾ��ȷ����
A��Na>Mg��Zn B��Na=Mg��Zn C��Mg��Zn >Na D��Na>Mg>Zn
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�������������꼶���£����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com