
| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
分析 (1)利用表中所给的数据来分析可以得出m的值;
(2)根据反应的化学方程式,由生成氨气的质量计算出样品中硝酸铵的质量,利用物质的质量分数的计算公式计算出硝酸铵的纯度;
(3)根据反应的化学方程式,由生成氨气的质量计算反应生成硝酸钠的质量,利用溶液中溶质的质质量分数的计算公式求算出硝酸钠的质量分数即可.
解答 解:(1)根据测定数据表中的时间与质量数据确定一些点,然后把各点利用平滑曲线图连接,从而可以判断出m的值大约为1.0;
(2)放出1.7g氨气消耗硝酸铵的质量为x,生成硝酸钠的质量为y,则:
NH4NO3+NaOH $\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+H2O+NH3↑
80 85 17
x y 1.7g
$\frac{80}{x}=\frac{85}{y}=\frac{17}{1.7g}$
解得:x=8g,y=8.5g,
(2)硝酸铵样品的纯度=$\frac{8g}{10g}$×100%=80%;
(3)所以反应后硝酸钠的质量分数为:$\frac{8.5g}{10g+80g+13.7g-1.7g-(10g-8g)}$×100%=8.5%.
答:反应后所得溶液的溶质质量分数为17%.
故答案为:
(1)1.0;
(2)80%;
(3)反应后所得硝酸钠溶液的溶质质量分数为8.5%
点评 本题关键是计算出反应后的溶液的质量,根据质量守恒定律,反应后所得硝酸钠溶液的质量=样品质量+溶解所加水的质量+氢氧化钠浓溶液的质量-反应放出氨气的质量-样品中的杂质的质量.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
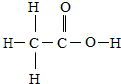 结构式是用元素符号和短线表示化合物(或单质)分子中原子的排列和结合方式的式子.如图所示醋酸的结构式,判断下列叙述正确的是( )
结构式是用元素符号和短线表示化合物(或单质)分子中原子的排列和结合方式的式子.如图所示醋酸的结构式,判断下列叙述正确的是( )| A. | 醋酸由四种元素组成 | |
| B. | 醋酸中还有两个碳原子、四个氢原子和两个氧原子 | |
| C. | 醋酸中碳原素的质量分数为53.3% | |
| D. | 醋酸是由醋酸分子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | NaCl(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | ZnCl2溶液(CuCl2溶液) | 加铁粉、过滤 |
| C | Fe(Zn) | 加过量FeSO4溶液、过滤 |
| D | H2SO4(HNO3) | 加Ba(NO3)2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可能是纯净物 | B. | 可能由CO与O2组成 | ||
| C. | 可能由CO与CO2组成 | D. | 可能由CO与O3组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是实验室常用的两个气体制备、收集、净化的多种功能装置.
如图是实验室常用的两个气体制备、收集、净化的多种功能装置.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是按元素周期表(局部)提供的信息.下列有关说法错误的是( )
如图是按元素周期表(局部)提供的信息.下列有关说法错误的是( )| A. | 铍和镁化学性质相似 | B. | 铝原子的核内有13质子 | ||
| C. | Na和Mg2+的核外电子数相同 | D. | Na、Mg、Al的金属活动性逐渐减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com