
【题目】下图是某同学设计的“自过滤”器,能在无人在场的情况下实现顺利过滤,其中装置的关键是导管a和b的设计,下列设计能达到“自过滤”目的的是
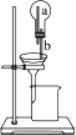
A. a的上端应该在圆底烧瓶中的液面以上,b的下端应在漏斗中的滤纸边缘以上
B. a的上端应该在圆底烧瓶中的液面以下,b的下端应在漏斗中的滤纸边缘以上
C. a的上端应该在圆底烧瓶中的液面以上,b的下端应在漏斗中的滤纸边缘以下
D. a的上端应该在圆底烧瓶中的液面以下,b的下端应在漏斗中的滤纸边缘以下
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】(实验探究)在如图所示,将O2、CO2、湿度(测水蒸气)传感器探头放入有少量空气的保鲜袋中,打开仪器开始采集数据,然后向袋内呼出气体。采集的数据如图所示,纵坐标均为某气体体积分数(%),横坐标均为时间(S)。据图回答下列问题:
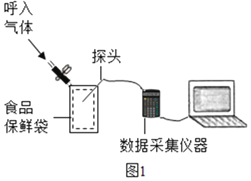
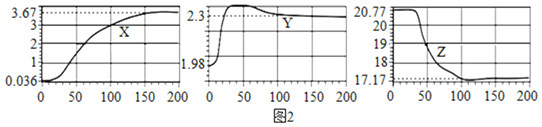
(1)表示O2体积分数变化的曲线是______(选填“X”、“Y”、“Z”)。
(2)根据如图在实验中200s时没有采集数据的其余气体的总体积分数为______。
(3)Y曲线60s之后逐渐下降,可推测保鲜袋中可能出现的现象是______。
(反思拓展)
(1)小组同学曾认为空气成分中“其它气体和杂质”主要包括水蒸气等,由实验可判断该认识是错误的,理由是由实验可知,空气中水的体积分数为1.98%,而空气成分中其它气体和杂质体积分数只有______。
(2)为了能保持载人飞行的飞船座舱内空气成分的稳定,科学家设想的方案是:不断把座舱内空气通过盛有过氧化钠的容器,并把处理后的气体重新充入座舱。其中过氧化钠的作用是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)请在Ca、H、O、S四种元素中任意选择三种元素组成合适的物质:①一种盐的化学式为__;②组成的两种化合物相互之间可以发生中和反应,其反应的化学方程式为:__。
(2)如图是盐酸和氢氧化钠溶液反应过程中溶液pH的变化曲线:
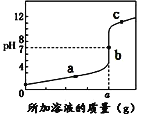
①该实验操作是将__溶液滴加到另一种溶液中;
②当溶液处于a点时,所得溶液中的溶质为(写化学式)___;
③若甲、乙两同学在实验时,反应后的溶液分别处于a点和c点状态,丙同学欲判断他们的实验情况,在没有指示剂的情况下,他可以用a.铁粉b.硝酸银溶液c.碳酸钠溶液中的___帮助确定(填字母)。
(3)某同学欲从含泥沙的粗盐(氯化钠和泥沙的混合物)中提纯氯化钠并计算提纯的产率,试回答:

操作①需要用到的玻璃仪器有玻璃棒、烧杯、__,该步骤中玻璃棒作用是__。若最终提纯获得的NaCl产率偏低,原因可能是___(填字母编号)。
A 粗盐没有完全溶解 B 滤纸破损
C 过滤器中的液面高于滤纸边缘 D 蒸发时没有用玻璃棒搅拌。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象分别与选项中的实验现象及结果相对应,其中正确的是( )
A.  电解水
电解水
B. 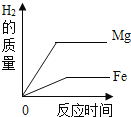 将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
C. 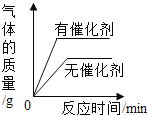 等体积、等溶质质量分数的过氧化氢溶液制取氧气
等体积、等溶质质量分数的过氧化氢溶液制取氧气
D. 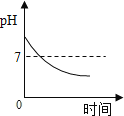 服用胃舒平
服用胃舒平![]() 主要成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
主要成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是生产、生活中应用很广泛的一种金属.下列是与铁的性质有关的部分实验图,请回答下列问题.

(1)A中细铁丝燃烧生成黑色固体物质的化学式是______.
(2)B中铁钉最易生锈的部位是______(填“a”、“b”或“c”).
(3)C中试管内充分反应后的溶液呈______色,发生反应的化学方程式是______.
(4)D中反应一段时间后,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比______(填“增大”、“不变”或“减小”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年三月五号,十三届人大二次会议在北京人民大会堂开幕。从李克强总理的政府报告中我们能深切体会到国家对于环境保护、环境治理的高度重视。在工业生产上规定空气中二氧化硫的允许排放量不得超过![]() ,否则将危害人类的健康,造成环境污染。某校学习小组欲利用“碘量法”测定扬州石化厂附近空气中的
,否则将危害人类的健康,造成环境污染。某校学习小组欲利用“碘量法”测定扬州石化厂附近空气中的![]() 的含量,请你参与并协助他们完成相关学习任务(部分装置图如下图所示)。
的含量,请你参与并协助他们完成相关学习任务(部分装置图如下图所示)。
(查阅资料)淀粉遇碘(![]() )变蓝,遇氢碘酸(
)变蓝,遇氢碘酸(![]() )不变色.氢碘酸为无色液体.
)不变色.氢碘酸为无色液体.
(测定原理)碘溶液吸收![]() 的化学反应原理是:
的化学反应原理是:![]()
(测定步骤)
①先准确称取1.27g粉末状碘(![]() ),并称取一定量的碘化钾(碘化钾可增大碘在水中的溶解度),加水使之完全溶解,配成1000mL碘水,准确称量取此溶液5.00mL并稀释10倍,再滴加2~3滴淀粉指示剂既得标准碘溶液。
),并称取一定量的碘化钾(碘化钾可增大碘在水中的溶解度),加水使之完全溶解,配成1000mL碘水,准确称量取此溶液5.00mL并稀释10倍,再滴加2~3滴淀粉指示剂既得标准碘溶液。
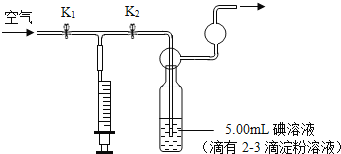
②准确量取标准碘溶液5.00mL倒入洗气瓶中待用(如上图)。则该标准碘溶液中所含碘的溶质质量分数为____________(本题中溶液的密度可看做1.0g/cm3)
③到指定的测试地点甲处抽气,抽气时应先关闭旋塞K2,打开旋塞K1,拉注射器活塞到100mL处,再_______________将气体缓缓全部推入标准碘溶液中,即完成一次抽气。每次抽气100mL,直到反应恰好完全反应为止,记录抽气次数(n)。
④在测试地点甲处,有三位同学分别做了实验,实验数据如下
测试地点甲处 | 小青 | 小白 | 小金 |
抽气次数n | 88 | 91 | 85 |
数据中__________(选填:小青、小白或小金)的最接近真实值,另两位同学不准确的原因为__________________。
⑤小组的其他同学再到不同地点再重复实验4次(每次所取碘溶液均为5.00mL)。这样做的目的是____________。5次实验的抽气次数记录见下表
测试地点 | 甲处 | 乙处 | 丙处 | 丁处 | 戊处 |
抽气次数 | 85 | 89 | 80 | 92 | 79 |
(交流与讨论)
(1)所配制的碘溶液显______色,实验中表明恰好完全反应的现象是__________。
(2)所配制的碘溶液浓度过浓,过稀都不合理,试分析浓度过浓不合理的原因是_________。
(3)通过计算,学习小组得出结论:扬州石化厂附近空气中![]() 的含量为____mg/l______(选填“超标”或“不超标”)
的含量为____mg/l______(选填“超标”或“不超标”)
(4)化工厂的含硫尾气处理后才能排放,下列物质中,能吸收![]() 的有______(选填字母)。
的有______(选填字母)。
A 氨水
B 酸性高锰酸钾溶液
C 熟石灰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用二氧化锰催化过氧化氢溶液分解的方法制取氧气。该实验速率快,产物无污染,某实验小组进行了如下探究。
(探究实验)书本介绍了除了用二氧化锰外,硫酸铜溶液也可以催化过氧化氢溶液的分解,查阅资料得知,氯化铁溶液也可以催化过氧化氢溶液的分解。那么,硫酸铜溶液和氯化铁溶液催化的效果怎么样呢?请根据下表四组实验现象,回答下面问题
序号 | 催化剂 | 实验步骤 | 实验现象 | 实验结论 |
1 | FeC13溶液 | 向5mL4%的H2O2溶液,滴5滴0.1%FeC13溶液 | 试管中产生大量气泡 | FeC13溶液对H2O2的分解有较好的催化效果 |
2 | FeC13溶液 | 向5mL12%的H2O2溶液,滴5滴0.1%FeC13溶液 | 试管中有适量气泡 | |
3 | CuSO4溶液 | 向5mL4%的H2O2溶液,滴5滴0.1%CuSO4溶液 | 试管中产生少量气泡 | CuSO4溶液对H2O2的分解催化效果一般 |
4 | CuSO4溶液 | 向5mL12%的H2O2溶液,滴5滴0.1%CuSO4溶液 | 试管中气泡量很少 |
(思考分析)
(1)CuSO4属于______(填“酸”或“碱”或“盐”)
(2)请你写出用二氧化锰催化过氧化氢溶液分解的反应方程式______。
(3)通过实验____(填序号)可以比较硫酸铜溶液和氯化铁溶液催化过氧化氢溶液分解的效果。
(4)请你从上面的实验,选择一组合适的药品进行实验室制取氧气,____%H2O2溶液,______(填催化剂的种类和浓度)。
(5)从上面的实验中,你还能得到什么结论______。
(拓展延伸)
(6)在老师的鼓励下,同学们继续探究FeCl3溶液中到底是哪种粒子催化H2O2的分解,请你设计一组实验进行探究______。
(7)另一名同学了解到,加热也可促进过氧化氢溶液分解,于是进行如下实验,分别取5mL12%的H2O2溶液于试管中进行水浴加热,步骤和现象如下:
序号 | 加热耗时 | 水浴温度 | 分解现象 |
1 | 12分 | 65℃ | 少量气泡 |
2 | 15分 | 74℃ | 明显气泡 |
3 | 21分 | 87℃ | 大量气泡 |
根据该同学的探究,试分析回答,为什么实验室通常不用加热过氧化氢溶液的方法制氧气?(两点理由):______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:
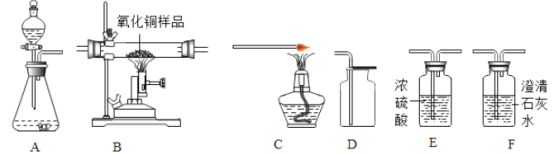
(1)若以石灰石和稀盐酸为原料在实验室中制备并收集干燥的二氧化碳。
①所选仪器的连接顺序为_____(从左到右填写装置序号字母)。
②生成二氧化碳时,所发生反应的化学方程式为_____。
③若将二氧化碳通入澄清石灰水中,石灰水的pH将_____(填“变大”“变小”“不变”之一)。
(2)欲用纯净的一氧化碳气体,测定某不纯氧化铜样品的纯度(CuO+CO![]() Cu+CO2,杂质不反应),并验证气体生成物的性质。某同学所选仪器装置的连接顺序为:纯净的一氧化碳→B→F→C。
Cu+CO2,杂质不反应),并验证气体生成物的性质。某同学所选仪器装置的连接顺序为:纯净的一氧化碳→B→F→C。
①连接仪器装置C的目的是_____。
②若氧化铜样品质量为30g,反应后B装置的质量减少5g,则该氧化铜样品中氧化铜的质量为_____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com