
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.设计实验证明金属的活动性顺序,可以使用活动性居中的金属为单质、强和弱的金属为盐溶液的方法,或是活动性居中的金属为盐溶液,强和弱的金属为单质的方法,也可以使用加酸观察是否产生气体的方法.
解答 解:在金属活动性顺序中,Fe>Cu>Ag,用实验方法探究Fe、Cu、Ag三种金属的金属活动性强弱,Fe,Ag三种金属的活动性,可将Fe和Ag放入 Cu(NO3)2或者Cu(SO4)2溶液中,或者将Cu 伸入 Fe(NO3)2溶液和AgNO3溶液.
故答为:Fe,Ag,Cu(NO3)2或者Cu(SO4)2;Cu,Fe(NO3)2,AgNO3.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源: 题型:解答题
 小明记得在学习金属活动性顺序的应用时,老师曾说过一般不会用K、Ca、Na等活泼金属和盐溶液进行置换反应,因为这些金属能直接和水发生反应生成对应的碱和氢气.小明查阅资料如下:
小明记得在学习金属活动性顺序的应用时,老师曾说过一般不会用K、Ca、Na等活泼金属和盐溶液进行置换反应,因为这些金属能直接和水发生反应生成对应的碱和氢气.小明查阅资料如下:| 实验方案 | 实验现象 | |
| 甲 | 将磁铁靠近黑色粉末 | 黑色粉末可被磁铁全部吸引 |
| 乙 | 取少量黑色粉末加入稀盐酸中 | 有气泡 |
| 实验方案 | 实验现象 | 结论或化学方程式 |
| 1、取实验后的黑色粉末,加入足量的A溶液,搅拌使反应充分. | 黑色物质表面有红色物质,溶液颜色出现较浅的绿色,烧杯底部仍有较多黑色物质 | Fe+CuSO4=FeSO4+Cu |
| 2、过滤、洗涤、干燥,再用磁铁吸引 | 黑色物质可被磁铁全部吸引,留下红色固体 | 被磁铁吸引的物质是铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH | B. | MgCl2 | C. | Na2CO3 | D. | CaO |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 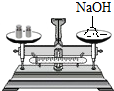 称16.5g氢氧化钠 | B. | 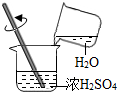 稀释浓硫酸 | ||
| C. | 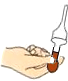 滴管的使用 | D. | 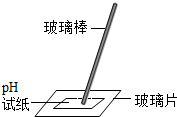 测溶液的pH值 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
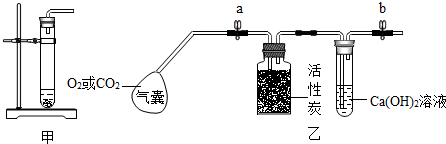
 用图中的装置可进行气体和固体的反应.
用图中的装置可进行气体和固体的反应.| 组别 | 固体 | 气体 | 装置内发生反应的化学方程式 |
| 1 | |||
| 2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
| 称量项目 | 称量时间 | 电子天平试样足量稀盐酸 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com