
【题目】下图是初中化学的些基本实验,请回答相关问题:
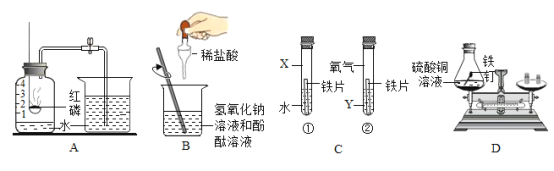
(1) A实验是测定空气中氧气含量,实验操作过程为:在集气瓶内加入少量水,并将水面上方空间分为5等份,接下来的实验步骤依次为____________(填序号), 最后打开弹簧夹。
①冷却到室温
②用弹簀夹夹紧橡皮管
③点燃燃烧匙中的红磷,立即伸入瓶中并塞紧瓶塞。
(2) B实验是探究中和反应,实验中证明反应发生的现象是______________。
(3) C实验是探究氯化钠能否加快铁的锈蚀速率,试管①中物质X和试管②中的物质Y分别是______________。
(4)随着科学研究的进展,化学实验方法也从定性到定量发生了质的转变。若按此实验方法分类,应将验证质量守恒定律的D实验和______________(填 “A”、“B”或“C”) 实验分为一类。
【答案】②③① 红色溶液逐渐消失(或溶液由红色变成无色等合理表述) 氧气、食盐水(或氯化钠溶液) A
【解析】
(1)测定空气中氧气含量实验:在集气瓶内加入少量水,并将水面上方空间分为5等份,用弹簧夹夹紧橡皮管,点燃燃烧匙中的红磷,立即伸入瓶中并塞紧瓶塞,冷却到室温打开止水夹,故实验步骤依次为②③①。故答案为:②③①;
(2)B实验氢氧化钠与盐酸反应生成氯化钠和水,氢氧化钠溶液使酚酞变红,氯化钠溶液呈中性,酚酞溶液呈无色,当看到溶液由红色变为无色说明二者发生了中和反应。故答案为:红色溶液逐渐消失(或溶液由红色变成无色等合理表述)
(3)C实验探究氯化钠能否加快铁的锈蚀速率,需做对照实验,变量是水和食盐水,因此试管①中物质X为氧气,试管②中的物质为食盐水。故答案为:氧气、食盐水(或氯化钠溶液);
(4)定量实验是从数值、数量上进行分析。验证质量守恒定律、利用红磷测定空气中氧气含量的实验,均属于定量实验。故答案为:A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】化学与生活息息相关
(1)蛋白质是人体不可缺少的营养物质,各种蛋白质在维持人的生命活动中起着极其重要的作用,是细胞的基础物质。下图物质中含蛋白质的是_______。

(2)“食品安全”是一个永恒的话题。你认为下列认识科学的是_________(填字母)。
A任何食品都不可以使用食品添加剂
B霉变的大米、花生,即使经过蒸煮也不能食用
C用聚乙烯塑料包装食品
D用亚硝酸钠代替食盐来腌渍食品
(3)牛奶含有“钙,铁、锌、钠”是指______(填“元素”或“单质”)。其中属于微量元素的是______,人体缺_______会引起智力底下,甚至侏儒症。
(4)材料对我们生活的影响越来越大。
合金具有许多良好的物理、化学和机械性能。合金的硬度一般比各成分金属______(填“大”或“小”),多数合金的熔点_____(填“高”或“低”)于组成它的成分金属。郊外通常比较泥泞,如果你的交通工具是自行车,铁质部件容易生锈。铁锈蚀的条件是铁与氧气和______共同接触。铁锈的主要成分是_______(填化学式)。你回来进行清洗后是如何防锈的: _____(填字母)。
A立即晾晒干B链条传动部件涂上油C涂油漆
下列常见材料中属于复合材料的是______。(填序号)
①陶瓷 ②有机玻璃 ③铝合金 ④铝塑条 ⑤玻璃钢
(5)人类社会离不开能源
当今社会,人类利用的能源主要来源于化石燃料,它是一种______(填“不可”或“可”)再生能源。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上,高温煅烧石灰石可制取生石灰(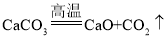 )。现有100g CaCO3样品,高温锻烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是
)。现有100g CaCO3样品,高温锻烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是
A.反应后固体质量减少的原因是逸出了二氧化碳气体
B.生成物中CaO的质量是42g
C.剩余固体中钙元素的质量分数大于40%
D.剩余固体中碳元素与氧元素的质量之比大于1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验创新是重要的学科素养。小明用W形玻璃管完成了课本上的两个实验。
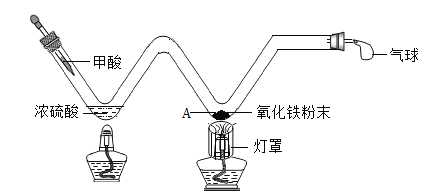
(1)探究炼铁原理如图:甲酸(HCOOH)在热的浓硫酸的作用下,分解生成一氧化碳和水,该反应的化学方程式是________,实验时,酒精灯加灯罩的作用是_________,A处可观察到的现象是__________。
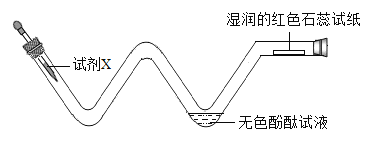
(2)探究微粒性质如图:加入试剂X,观察到无色酚酞试液变红,红色石蕊试纸变蓝。试剂X可能是______,该装置的优点是______(答一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
![]()
0
(1) M点表示的含义是___________________。
(2) 50°C时,将40g甲物质加入到50g水中,充分溶解后,所形成的溶液中溶质与溶剂的质量比为_______________。
(3) 20°C时,处于a点状态的甲溶液,升温至50°C时,所得溶液中溶质质量分数_____________(填“变大”、“变小”或“不变”)。
(4)分别将50°C甲、乙、丙三种物质的饱和溶液100g降温到20°C时,所得溶液的质量由大到小的顺序是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理如下:
①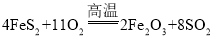
②
③![]()
④
下列说法不正确的是( )
A. 反应①②④均有元素化合价发生变化
B. 反应①④不属于四种基本反应类型中的任何一种
C. 反应②③属于化合反应
D. 四个反应的产物都有氧化物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学,初中化学课上做过许多实验,根据下列四个实验,回答问题:
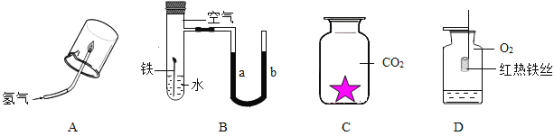
(1)A实验中先_____,再点燃氢气,以免发生爆炸,氢气燃烧的化学方程式是______。
(2)B实验中开始时U型管两端的红墨水液面相平,一段时间后,能观察到的现象是___________。
(3)将白纸剪的五角星用紫色石蕊试液喷湿,放入集气瓶C中,观察到的现象是____,用化学方程式表示产生这种现象的原因___________。
(4)集气瓶D中的铁丝没有燃烧,从燃烧条件来说,原因是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。已知:温度过高过氧化物会分解生成氧化物和氧气。
方法 1:由Ca(OH)2为原料最终反应制得,其制备流程如图:
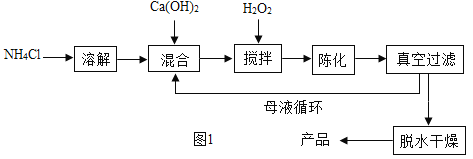
方法 2:由鸡蛋壳(含CaCO3高达 90%)为原料最终反应制得,其制备流程如图:
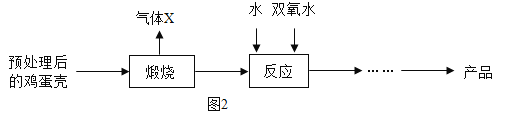
(1)方法 1 中搅拌的目的是_____。请将搅拌过程中发生反应的化学方程式补充完整![]() _____
_____![]() .制备过程中除水外可循环使用的物质是_____(填化学式)。
.制备过程中除水外可循环使用的物质是_____(填化学式)。
(2)方法 2 中气体 X 是_____,实验室常用_溶液来吸收。煅烧后的反应是化合反应,也能生成CaO28H2O,反应的化学方程式为_____。该反应需控制温度在 0~2℃,可将反应器放置在_,获得的CaO2产品中主要含有的固体杂质是_(填化学式)。
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能_____。
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO28H2O的反应符合“绿色化学”的是________(填“方法 1”或“方法 2”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“太阳能光伏发电系统”在交通、通讯、海洋、气象、光伏电站、太阳能建筑等领域中,具有不同程度的应用。白天在太阳光照条件下,太阳能电池组件产生一定的电动势,对太阳能电池方阵中的蓄电池进行充电,将电能储存起来,晚上,将直流电转换成交流电,输送到配电柜进行供电。请回答下列问题:

(1)“太阳能光伏发电系统”在白天时工作过程中的能量转化是(用“→”表示转化)_____。
(2)该系统组成中的边框为铝合金制成,也是太阳能发电中最重要的部分,该材料具有抗机械冲击力好等性能,你认为该材料还应具备的物理性质是_____(填字母)。
A 密度小,抗腐蚀性好 B 熔点高,导电性好 C 强度高、密度小
(3)有科学家设想把太阳能光伏系统安装在家用车上,如果实现可以部分解决_____能源面临耗尽的问题,同时减少了_____等污染物的排放(填两种物质)。
(4)该系统组成的支架所用的钢材长时间使用后,需要对其表面进行处理,若用盐酸洗会产生“酸洗废液”(主要成分为FeCl2),工业上将“酸洗废液”在高温下与氧气、水反应制得氧化铁,同时产生氯化氢气体,写出此反应的化学方程式_____,反应前后铁元素的化合价分别为:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com