
| 被检物 | 所用试剂 | 写出有关化学方程式 |
| 盐酸与稀硫酸 | BaCl2溶液 | H2SO4+BaCl2=BaSO4↓+2HCl |
| 生石灰与石灰石 | 稀HCl | CaCO3+2HCl=CaCl2+H2O+CO2↑ |
分析 (1)盐酸与氯化钡不反应,硫酸与氯化钡反应生成硫酸钡白色沉淀,据此分析;
(2)石灰石能够和盐酸反应产生二氧化碳气体,而氧化钙反应无现象,据此分析.
解答 解:(1)盐酸与氯化钡不反应,两种溶液混合没有现象;硫酸与氯化钡反应生成硫酸钡白色沉淀和盐酸,所以用氯化钡能够鉴别盐酸和硫酸;
故答案为:BaCl2溶液;H2SO4+BaCl2=BaSO4↓+2HCl;
(2)石灰石能够和盐酸反应产生二氧化碳气体,而氧化钙反应无现象,所以用稀盐酸能够鉴别生石灰和石灰石;
故答案为:稀HCl;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题考查了常见物质的鉴别,在解此类题时,首先分析需要鉴别的物质的性质,然后选择适当的试剂,出现不同的现象即可鉴别.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
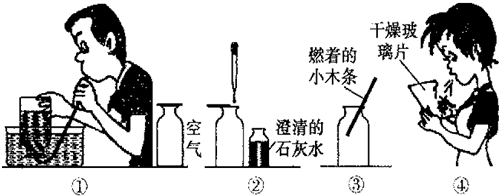
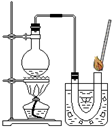 小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeCl3、NaOH、NaCl | B. | Na2SO4、HCl、BaCl2 | ||
| C. | CuSO4、KCl、HCl | D. | Na2CO3、NaCl、Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
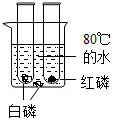 为了探究燃烧的条件,小军查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,五氧化二磷刺激人的呼吸道.他设计了如图所示的实验装置.[将分别盛有少量的白磷和少量红磷的两支试管,放人到盛水的烧杯中,另将少量白磷直接投入到烧杯的水中.观察到的实验现象如下:
为了探究燃烧的条件,小军查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,五氧化二磷刺激人的呼吸道.他设计了如图所示的实验装置.[将分别盛有少量的白磷和少量红磷的两支试管,放人到盛水的烧杯中,另将少量白磷直接投入到烧杯的水中.观察到的实验现象如下:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeO+H2SO4═4FeSO4+H2O | B. | Fe2O3+6HCl═2FeCl3+3 H2O | ||
| C. | Fe2O3+2H2SO4═2FeSO4+2 H2O | D. | Fe2O3+3H2SO4═Fe2(SO4)3+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com