
分析 (1)银离子和氯离子能够结合成氯化银沉淀;
(2)化合物中元素化合价代数和为零;
有元素化合价升降的化学反应属于氧化还原反应;
(3)根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)判断自来水是否消过毒的方法:向自来水中加入硝酸银溶液,有白色沉淀生成,证明自来水消过毒,反之则没有消毒.
故填:向自来水中加入硝酸银溶液,有白色沉淀生成,证明自来水消过毒,反之则没有消毒.
(2)次氯酸的化学式为HClO,其中H为+1价、O为-2价,设Cl元素化合价为x,则(+1)+x+(-2)=0,
解得x=+1;
Cl2+H2O═HClO+HCl中,氯元素化合价由0变成+1和-1,属于氧化还原反应.
故填:+1;氧化还原.
(3)消毒用的氯气常用电解饱和食盐水的方法来生产(2NaCl+2H2O═2NaOH+H2↑+Cl2↑).若某地区需500万吨自来水,则要消耗饱和食盐水多少吨?(列式计算,最后的结果取整,已知该生产条件下食盐溶解度为36克).
(3)设理论上应消耗氯化钠的质量为x,
500万吨水中应该加入氯气的质量为:5000000000kg×0.002g/kg=10000000g=10t,
2NaCl+2H2O═2NaOH+H2↑+Cl2↑,
117 71
x 10t
$\frac{117}{x}$=$\frac{71}{10t}$,
x=16.5t,
设需要消耗饱和食盐水的质量为y,
根据题意有:y×$\frac{36g}{100g+36g}$×100%=16.5t,
y=62.3t,
答:若某地区需500万吨自来水,则要消耗饱和食盐水62.3t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:实验探究题
 兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:
兴趣小组的同学为研究酸和碱反应的特点,将稀盐酸匀速、缓慢地滴入盛有氢氧化钠溶液的烧杯中,并测绘出烧杯内溶液的温度和pH的变化图象(如图所示),请回答问题:| 主要成分 (均占药片质量的95%) | 主要成分的 相对分子质量 | 建议每次 服用剂量/g |
| Al(OH)3 | 78 | 0.25 |
| NaHCO3 | 84 | 0.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
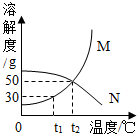 溶解度是解决溶液相关问题的重要依据,请根据如图溶解度曲线解决下列问题.
溶解度是解决溶液相关问题的重要依据,请根据如图溶解度曲线解决下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫(SO2) | 7 | ||
| 二氧化氮(NO2) | 24 |
| A. | 焚烧垃圾 | B. | 汽车排放尾气 | ||
| C. | 用煤和石油产品作燃料 | D. | 生活污水未经处理直接排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com