
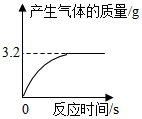
 实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图.
实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量和反应时间关系如图.分析 (1)根据催化剂的特点分析;
(2)根据影响反应进行的因素分析;
(3)根据生成气体的质量与反应时间的关系图,可得知所取过氧化氢完全反应放出氧气质量为3.2g,利用反应放出氧气的质量可计算所取溶液中过氧化氢的质量,则可计算该溶液中溶质的质量分数.
解答 解:(1)过氧化氢在二氧化锰的催化下生成水和氧气,所以反应后固体为二氧化锰,又因为催化剂反应前后质量和化学性质都不变,所以完全反应后,经过滤、烘干,得到固体的质量为1g,故填:1g;
(2)A、二氧化锰作为催化剂反应前后质量和化学性质都不变,故错误;
B、反应物的浓度越小,反应速率越小.故正确;
C、温度越高,反应速率越大,故错误;
故选:B
(3)设过氧化氢溶液中溶质的质量为x.
2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
$\frac{68}{x}=\frac{32}{3.2g}$
x=6.8g
该溶液中溶质的质量分数=$\frac{6.8g}{100g}$×100%=6.8%
答:该溶液中溶质的质量分数为6.8%.
点评 本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.


 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:初中化学 来源: 题型:填空题
 分析处理图表信息是学习的一种重要方法,如表是氯化钠和硝酸钾在不同温度下的溶解度.
分析处理图表信息是学习的一种重要方法,如表是氯化钠和硝酸钾在不同温度下的溶解度. | 温度/℃ | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用稀盐酸除铁锈 Fe2O3+6HCl═2FeCl2+3H2O 复分解反应 | |
| B. | 石笋、石柱的形成 CaCO3+H2O+CO2═Ca(HCO3)2 化合反应 | |
| C. | 用含氢氧化镁的药物治疗胃酸过多症:Mg(OH)2+2HCl=MgCl2+2H2O 复分解反应 | |
| D. | 证明锌比银活泼 Zn+2AgCl═ZnCl2+2Ag 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
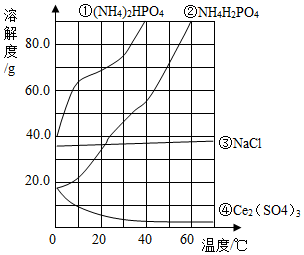 如图为四种物质的溶解度曲线,则下列说法错误的是( )
如图为四种物质的溶解度曲线,则下列说法错误的是( )| A. | 当温度为10℃时,物质溶解度关系为①>③>②>④ | |
| B. | 若NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶 | |
| C. | 在10℃时把NH4H2PO4和Ce2(SO4)3的饱和溶液升温到30℃,有晶体析出的是Ce2(SO4)3 | |
| D. | 22℃时(NH4)2HPO4饱和溶液的质量分数约为70% |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气点燃前需验纯,则点燃任何可燃性气体前都需验纯 | |
| B. | 含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质不一定含碳元素 | |
| C. | 单质由同种元素组成,由同种元素组成的物质一定是单质 | |
| D. | 室温下pH<7的溶液呈酸性,同理pH<7的雨水是酸雨 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用小苏打除去面团发酵产生的酸 | B. | 用白醋长时间浸泡铝壶内的水垢 | ||
| C. | 用食盐除去铁锅内的油污 | D. | 用燃着的火柴检查煤气罐是否漏气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
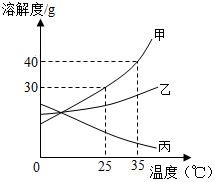 甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com