
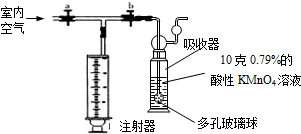
 我国规定居室中装修材料释放出的甲醛气体含量不得超过0.08mg/m3.某研究小组通过查阅资料,拟采用“酸性高锰酸钾溶液褪色法”来测定居室中的甲醛气体含量.测定原理是:5X+4KMnO4+6H2SO4═2K2SO4+4MnSO4+5CO2↑+11H2O(X代表甲醛).操作过程为:用容积为1000mL的医用注射器抽取空气,缓慢注入酸性高锰酸钾溶液中(装置如下,a、b为止水夹),多次注气后当高锰酸钾溶液正好褪色时,停止注入.
我国规定居室中装修材料释放出的甲醛气体含量不得超过0.08mg/m3.某研究小组通过查阅资料,拟采用“酸性高锰酸钾溶液褪色法”来测定居室中的甲醛气体含量.测定原理是:5X+4KMnO4+6H2SO4═2K2SO4+4MnSO4+5CO2↑+11H2O(X代表甲醛).操作过程为:用容积为1000mL的医用注射器抽取空气,缓慢注入酸性高锰酸钾溶液中(装置如下,a、b为止水夹),多次注气后当高锰酸钾溶液正好褪色时,停止注入.分析 (1)根据化学反应4KMnO4+5X+6H2SO4=2K2SO4+4MnSO4+5CO2↑+11H2O,利用质量守恒定律来推出X的化学式;
(2)根据装置的特点选择状态及推断测量结果;
(3)根据高锰酸钾的质量计算甲醛的质量,然后计算空气中甲醛的含量和标准进行比较得出结论.
解答 解:(1)化学反应4KMnO4+5X+6H2SO4=2K2SO4+4MnSO4+5CO2↑+11H2O,遵循质量守恒定律,则反应前后的元素相同,原子个数相等,K、Mn、S元素的原子个数前后相等,
反应前现有40个O原子,而反应后共45个O原子,则X中共5个O原子,
反应前现有12个H原子,而反应后共有22个H原子,则X中共有10个H原子,
反应前没有C原子,而反应后共有5个C原子,则X中共有5个C原子,
又X的化学计量数为5,则X的化学式为CH2O.
故答案为:CH2O
(2)向酸性KMnO4溶液注气时,两个止水夹的状态应a关b开;如果注气过快,可能有些气体来不及被吸收,会使测定结果偏小;
故答案为:a关b开;小
(3)解:设甲醛的质量为x
4KMnO4 +5CH2O+6H2SO4 =4MnSO4+2K2SO4+5CO2↑+11H2O
632 150
7.9g×0.001% x
$\frac{632}{7.9g×0.001%}$=$\frac{150}{x}$
x=4.0×10-6g=0.0004mg
因为每次用注射器抽取1000mL室内空气,第200次恰好反应,则通入的空气体积为:1000ml×200=200000mL=0.2m3,所以该居室内空气中甲醛的含量
$\frac{0.0004g}{{0.2m}^{3}}$=0.02mg/m3<0.08mg/m3,故甲醛不超标.
故答案为:甲醛不超标
点评 本题是有关室内甲醛含量的测定的探究,涉及的知识点较多:质量守恒定律的运用、根据化学式的计算、根据化学方程式的计算等,综合性较强,难度较大.


科目:初中化学 来源: 题型:解答题
 汽车是现代生活中不可缺少的工具之一.请回答下列问题:
汽车是现代生活中不可缺少的工具之一.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
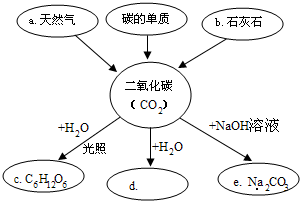 如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略)
如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 因素 | 第一组 | 第二组 | 第三组 | ||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80℃ |
| 加入溶剂种类 | 水 | 酒精 | 水 | 水 | 水 |
| 加入溶剂质量 | 20g | 20g | 10g | 10g | 10g |
| 加入固体种类 | 硝酸钾 | 硝酸钾 | 硝酸钾 | 食盐 | 硝酸钾 |
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g |
| 溶解固体质量 | 6.2g | 0g | 3.1g | 3.6g | 10g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com