
32.5 g锌可以跟150 g硫酸溶液恰好完全反应。计算:
(1)反应后溶液中溶质质量分数为多少?
(2)这种硫酸溶液中溶质质量分数是多少?
(3)100 g这种硫酸溶液稀释成质量分数为20%的稀硫酸,需加入多少克水?
解:设反应生成硫酸锌质量为x,放出氢气质量为y,消 耗硫酸质量为z
耗硫酸质量为z
Zn + H2SO4 = ZnSO4 + H2↑
65 98 161 2
32.5g z x y
65:161=32.5g:x ,解 之得 x=80.5g
之得 x=80.5g
65:2=32.5g:y ,解之得 y=1g
65:98=32.5:z ,解之得 z=49g  (1分)
(1分)
反应后所得溶液的溶质质量分数=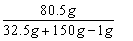 ×100%
×100% ≈44.4%; (1分)
≈44.4%; (1分)
反应的硫酸溶液中溶质质量分数=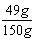 ×100%≈32.7%; (1分)
×100%≈32.7%; (1分)
(3)加水稀释,稀释前后溶质质量不变
设稀释成质量分数为20%的稀硫酸,需加入水质量为m
100g×32.7%=(100g+m)×20%,解之得m=63.5g (1分)
答:(1)反应后溶液中溶质质量分数为44.4%
(2)这种硫酸溶液中溶质质量分数是32.7%
(3)100 g这种硫酸溶液稀释成质量分数为20%的稀硫酸,需加入水63.5g。


科目:初中化学 来源: 题型:
李老师看同学们玩沙漏后,给同学们做了有趣的“水漏”实验(如图),两个大小相同的锥形瓶用长短不同的两个玻璃管连接,下方锥形瓶中有足量的几粒白磷,水温50℃,实验时将甲装置倒置变成乙,当乙装置中的水漏完后,用铁夹夹紧胶管后拔开下端变成丙,试回答:
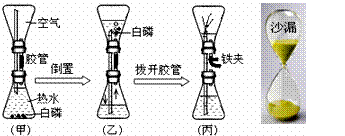
(1)乙实验看到上部锥形瓶中可能出现的现象是 ;甲和乙的实验探究的化学知识是 ;
(2)若乙实验能成功,丙实验就能形成喷泉,原因是 ;实验结束后,丙中进入上方锥形瓶的水最多不超过锥形瓶容积的 .
查看答案和解析>>
科目:初中化学 来源: 题型:
2005年10月12日,我国“神舟”六号载人飞船成功发射。航天飞船是用铝粉与高氯酸铵的混合物 的固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应:2NH4ClO4 = N2↑+ 4H2O + X + 2O2↑,则X的化学式为( )
的固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应:2NH4ClO4 = N2↑+ 4H2O + X + 2O2↑,则X的化学式为( )
A、HCl B、ClO2 C、Cl2 D、HClO
查看答案和解析>>
科目:初中化学 来源: 题型:
我市是重要的产棉区,棉农在种植棉花的过程中要适时适量地施用氮肥,下列肥料中属于氮肥的是( )
A、KCl B、Ca3(PO4)2 C、NH4HCO3 D、K2CO3
查看答案和解析>>
科目:初中化学 来源: 题型:
某校化学研究性学习小组的同学对一包因敞口放置已部分变质的氢氧化钠产生了兴趣,想通过实验测定其中碳酸钠的质量分数,请你参与他们的探究过程。
【提出问题】:样品中碳酸钠的质量分数是多少?
【知识准备】:
(1)氢氧化钠不能敞口放置的原因是: ;
(2)判断氢氧化钠是否变质的方法之一是向样品中加盐酸,反应的化学方程式是:
_________________________________________、______________________________________;
(3)判断氢氧化钠是否变质的另一种方法是将样品溶于水,再向样品中加澄清石灰水,看是否变浑浊,反应的化学方程式是:__ ________________________________________________.
________________________________________________.
(4)向氢氧化钠和碳酸钠混合物中加入盐酸时,盐酸先与氢氧化钠反应,再与碳酸钠反应;
【设计方案】:
甲组同学:称取16.40g样品,放入足量的盐酸直到反应 停止,共收集到4.40g二氧化碳。(设计思路:根据样品与盐酸反应生成二氧化碳的质量求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。)
停止,共收集到4.40g二氧化碳。(设计思路:根据样品与盐酸反应生成二氧化碳的质量求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。)
乙组同学:称取16.40g样品,加水配成溶液,再溶液中加入过量的澄清石灰水。过滤、洗涤、干燥,共得到白色沉淀10.00g。(设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。)
【解决问题】:
(1)乙组同学判断石灰水是否过量的方法是_____________________________________ __;
__;
(2)根据两组同学的实验结果,请你帮助他们计算出样品中碳酸钠的质量分数:
甲组同学:
乙组同学:
【交流与反思】:
在交流时,老师问同学们“能否用上述实验所得的数据计算出样品中氢氧化钠的质量分数”,甲乙两组的同学都一致认为可以。但小明思考后,觉得甲、乙两种方案都不妥,理由是:_______________________________________________;
小明又重新设计新方案:
【设计方案】:
先用电子秤准确称取16.40g变质的NaOH样品放入锥形瓶中,用电子秤秤得锥形瓶及样品的总质量为51.40g,再把175.00g 浓度为7.3%稀盐酸平均分成4份依次加入样品中,每次充分反应用电子秤秤得锥形瓶及所盛物质的质量,实验数据记录如下:
| 加入盐酸的次数 | 第一次 | 第二次 | 第三次 | 第 | 第五次 | 第六次 | 第七次 |
| 锥形瓶及所盛物质的总质量 | 76.40 | 101.40 | 126.40 | 151.40 | 174.20 | 197.00 | 222.00 |
【解决问题】:
请根据上述实验数据,计算样品中氢氧化钠的质量分数为_________________。(不要求写计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
2013年1月19日,首个《国际防治汞污染公约》发布。下图为元素汞的信息,从图中获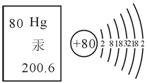 得的信息正确的一项是( )
得的信息正确的一项是( )
A.汞的核电荷数为80
B.汞属于非金属元素
C.汞的相对原子质量为200.6g
D.在化学反应中,汞原子容易得到电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com