
����Ŀ��ˮ�����౦�����Ȼ��Դ�������������������������أ�
��1���ж�������ˮ��Ӳˮ������ˮ���ɼ���_____���м��飮
��2�����о���ˮ�ĵ�һ�����У���Ծ����̶Ƚϸߵ���_____������ĸ����
A ���� B �������� C ���� D ����
��3����ͼΪ�ס����������ʵ��ܽ�����ߣ�
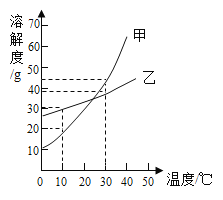
�ټס����������ʵ��ܽ�Ⱦ����¶ȵ����߶�_____������������������С������
��30��ʱ�������ʸ�ȡ25g���ֱ���100gˮ����ܽ⣬�ٰ�����Һ���µ�10�����о�����������_____������������Ϊ_____g��
�۵������ļס����������ʷֱ����30��ʱ�ı�����Һ����Ҫˮ��������С��ϵ�Ǽ�_____�ң�������������=������������
���𰸡�����ˮ C ���� �� 5 ��
��������
��1���ж�������ˮ��Ӳˮ������ˮ������ʹ�÷���ˮ���м��飬Ӳˮ�����ˮ��ϲ�������������ˮ��ϲ�����ĭ��
��2�������������Ծ����̶Ƚϸߵľ�ˮ������
��3���پ�ͼ���Կ������ס����������ʵ��ܽ�Ⱦ����¶ȵ����߶�����
��30��ʱ�������ʸ�ȡ25g���ֱ���100gˮ����ܽ⣬�ٰ�����Һ���µ�10�������ܽ�����¶ȵĽ��Ͷ���С�����о����������Ǽף���10��ʱ���ܽ����20g��������������Ϊ25g��20g=5g��
��30��ʱ���ܽ�ȴ����ҵ��ܽ�ȣ��ʵ������ļס����������ʷֱ����30��ʱ�ı�����Һ����Ҫˮ��������С��ϵ�Ǽ�С���ҡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ӧ�ù㷺��
��1�������������ֳ��������Ͻ��������ܲ������Ҫԭ����_____��ͬ��
��2��ͭп�Ͻ�������ƽ�Ϊ���ƣ�ʵ���������ϡ������𣬷�����Ӧ�Ļ�ѧ��ʽΪ_____��
��3�������йؽ�����˵������ȷ����_____��
A þ�ڿ�����ȼ�գ�����ҫ�۵İ⣬���ɰ�ɫ����
B Ϊ��ֹ�������⣬���������Ϳ�ͻ�ˢ���
C ͨ����̻��ķ���������ͭƬ��Ӳ�ȱȻ�ͭƬ��
D �������Ƚ���п����ʴ��˵��п�����Ľ������ǿ
��4����1000t��������80%�ij�����ʯ�������Ͽ�����������96%�������������Ƕ��٣�_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����22.3g Na2CO3��NaCl��������100gˮ��ʹ����ȫ�ܽ⣬�ټ���86.1g CaCl2��Һ��ǡ����ȫ��Ӧ�����˺����Һ198.4g�����㣺
��1�����ɳ����������Ƕ��ٿˣ�
��2����Ӧ��������Һ���������������Ƕ��٣������㾫ȷ��0.1%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�������ۡ�ľ̿�ۡ�þ����ɵĹ�������5g�������м���һ����������������ϡ����100g����ַ�Ӧ����ˣ��õ���Һ103.8g������1g������˵������ȷ���ǣ�������
A.����������������0.2g
B.��Һ��һ�������Ȼ�þ���Ȼ�����������
C.ϡ�����������������С�ڻ����7.3%
D.�������ijɷ���ľ̿�ۣ�������������þ��������Ϊ7��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ�й�����ת����ϵ�У������ʾ��dz��л�ѧ���������ʣ�����A���Ϻ�ɫ������B��C���Ԫ����ͬ��I��ij�������ϵ���Ҫ�ɷ֣���F��Һ����K����״���н�������ũҵ�ϳ��õ�ɱ����������Һ��ͼ�з�Ӧ��������ȥ��
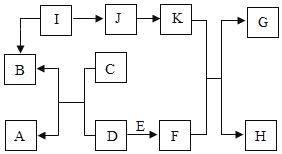
��1��I�Ļ�ѧʽ_____��
��2����Jת��ΪK�Ļ�����Ӧ����Ϊ_____��
��3��д��C��D��Ӧ�Ļ�ѧ����ʽ_____��д��K��F��Ӧ�Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����ɫ������Ʒ�������������ơ��������ơ�̼��ơ��Ȼ������Ȼ�þ�е�һ�ֻ���������ɣ�Ϊ̽������Ʒ����ɣ�ijС��ȡ������Ʒ���������̽���ʵ�飮
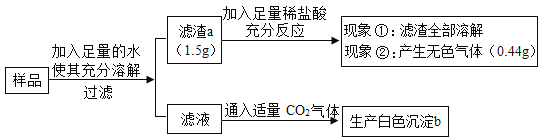
��ش��������⣺
��1�����˲������õ��IJ����������ձ�����������_____�����в�������������_____��
��2������a�ijɷ���_____����Һ�����ʵijɷֳ��Ȼ��ƻ���_____��
��3��������ʵ�������������Ʒ��һ��������_____��
��4���������������ȫ���ܽ�����Ϊ�����������ܽ������������䣬��ԭ��Ʒ�в���ȷ���Ƿ���ڵ�������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ҫ��Ҫ��Ӫ�����ʡ����A��B��������ѡ1����������������𣬼�һ����֡�
A | B |
(1)ֲ��������Ҫ�������������ס��������������������ָ___(���������)�� �ٵ��� �ڵ�Ԫ�� (2)��ľ���к���̼��أ����������ϡ���ľ������___��(������������������������)�� (3)����[CO(NH2)2]��һ�ָ�Ч���ʣ����е�Ԫ�����������ļ���ʽΪ____�� | (1)���ơ�����п�������彡��������Ҫ������ȱ�ƿ��ܻᵼ��___(���������)�� �����Ͳ� ��ƶѪ (2)��������(C6H10FeO6)�����������������������к�____��Ԫ�ء� (3)��ѧ���Ʋ��ܱ��Ͻ������������ÿ����Ҫ800��1200mg�ƣ�������ͼ��ʾ�ĸ�Ƭ���ƣ�ÿ������___Ƭ��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��װ�ã��ش��й����⣮
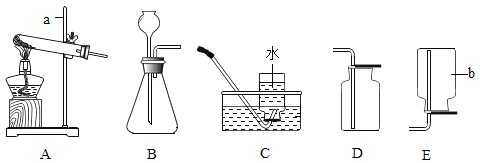
��1��д��ͼ������a��b�����ƣ�a_____b_____��
��2��ʵ������ȡ���ռ�������̼��Ӧѡ���װ����_____������ĸ������ѧ����ʽΪ_____��
��3��ʵ�����ü�������غͶ������̻������ȡ���ռ�������Ӧѡ���װ����_____������ĸ����
��4����װ�������Ӳ����ܺ���Ƥ�ܵIJ������ȰѲ����ܿ�_____��Ȼ�������������ɰѲ����ܲ��뽺Ƥ�ܣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ƽҵ������°������������Ƽ�����䲿�ֹ������£�
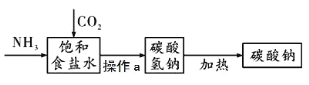
����Ҫ��Ӧԭ����
�� NaCl+H2O+NH3+CO2=NaHCO3��+NH4Cl
�� 2NaHCO3![]() Na2CO3+H2O+CO2�� �ȡ�
Na2CO3+H2O+CO2�� �ȡ�
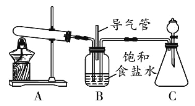
�������ϣ�ͨ������£�1L ˮ���ܽ�Լ 1L CO2 �� 700L NH3�� ij��ȤС���������ͼװ����ʵ����ģ����Ƽ���̣�����˵����ȷ����
���������Ƽ����ļ�ָ������������
�ڷ�Ӧԭ������Ӧ���������ܽ�ȵIJ���
����ͼ�У�B �е����ܵ�������ƽ����ѹ��C װ��������ȡ CO2
�ܸ��� NH3 �� CO2 �ܽ�ȵIJ�ͬ��Ϊ���ɸ���� NaHCO3��Ӧ����ͨ�� CO2 ��ͨ�� NH3
�ݲ��� a �������ǹ���
��Ӧԭ�����ʵ������� A װ���н���
��ҽ����NaHCO3 ����������θ�����
�෴Ӧ�����еĸ�����NH4Cl��ũҵ�ϳ��õĸ��Ϸ�
A.4 ��B.5 ��C.6 ��D.7 ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com