
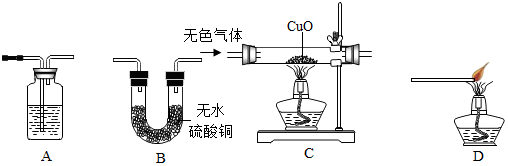
| 无色气体的成分 | 对应的实验现象 | ||
| 装置A中的液体 | 装置B中的固体 | 装置C中的固体 | |
| 猜想一:只有CO | 变浑浊 | 无明显现象 | 变红 |
| 猜想二:有一氧化碳和氢气 | 变浑浊 | 变蓝 | |
| 猜想三:只有H2 | 无变化 | 变蓝 | |
分析 根据一氧化碳能与氧化铜反应生成铜和二氧化碳,氢气能与氧化铜反应生成铜和水,检验二氧化碳使用的是澄清的石灰水,检验水使用的是无水硫酸铜,根据一氧化碳与铁的氧化物高温反应设计实验装置,根据数据结合物质间的反应进行分析解答即可.
解答 解:【设计实验】①检验二氧化碳使用的是澄清的石灰水,故填:石灰水;
②一氧化碳能与氧化铜反应生成铜和二氧化碳,氢气能与氧化铜反应生成铜和水,检验二氧化碳使用的是澄清的石灰水,检验水使用的是无水硫酸铜,需要先检验水的存在,再检验二氧化碳的存在,由于一氧化碳具有毒性,需要进行尾气处理,故填:CBAD;
【进行猜想】若是A中澄清石灰水变浑浊,则说明含有一氧化碳,若是B中变蓝,则说明含有氢气;故填:
| 无色气体的成分 | 对应的实验现象 | ||
| 装置A中的液体 | 装置B中的固体 | 装置C中的固体 | |
| 猜想一:只有CO | 变浑浊 | 无明显现象 | 变红 |
| 猜想二:有一氧化碳和氢气 | 变浑浊 | 变蓝 | |
| 猜想三:只有H2 | 无变化 | 变蓝 | |
点评 本题考查的是常见物质成分的推断,完成此题,可以依据物质的性质进行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:推断题
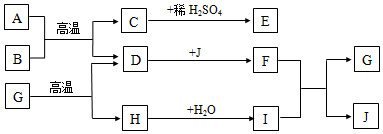
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
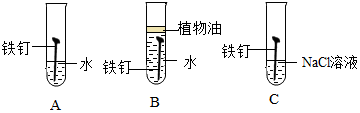
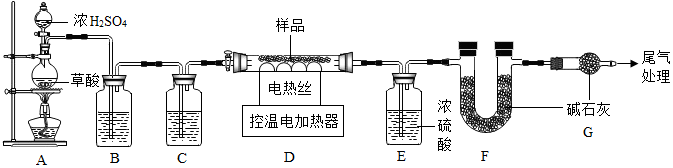
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 问题与猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 探究一:固体M是否失效 | 取适量固体M,加入盛有水的烧杯中,用温度计测量加入前后的温度 | 温度没有明显变化 | 固体M失效 |
| 探究二:固体M中是否含有氢氧化钙 | 将上述烧杯内的液体充分搅拌、静置,取上层清液,加入酚酞试液 | 溶液变红 | 有氢氧化钙 |
| 实验步骤 | 现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 材料:人类要在月球居住,首先离不开淡水和氧气,而月球上既没有水又没有空气.科学家发现月球的沙土中含有丰富的含氧钛铁矿,成分为TiO2、Fe2O3的混合物,若将这些矿石利用CO来还原可以提炼单质钛和铁,若用氢气还原,可以得到淡水.若将这些矿石通电,还可以从中分离出氧气.
材料:人类要在月球居住,首先离不开淡水和氧气,而月球上既没有水又没有空气.科学家发现月球的沙土中含有丰富的含氧钛铁矿,成分为TiO2、Fe2O3的混合物,若将这些矿石利用CO来还原可以提炼单质钛和铁,若用氢气还原,可以得到淡水.若将这些矿石通电,还可以从中分离出氧气.
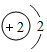
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 表示分子个数的是①③ | B. | 表示离子所带电荷数的是②⑤ | ||
| C. | 表示化合价数值的是④ | D. | 表示离子个数的是⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com