
分析 高锰酸钾受热分解后生成锰酸钾、二氧化锰和氧气,由于氧气逸出,所以反应后固体质量会减少;根据质量守恒定律可知,固体质量的减少量即为生成氧气的质量,然后根据反应方程式由氧气的质量求出参加反应的高锰酸钾的质量、生成锰酸钾的质量、二氧化锰的质量.
解答 解:(1)由质量守恒定律可知氧气的质量=10g-9.36g=0.64g;
(2)设参加反应的KMnO4质量为x,反应生成的K2MnO4质量为y、MnO2质量分别为z.
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 197 87 32
x y z 0.64g
$\frac{316}{x}=\frac{197}{y}=\frac{87}{z}=\frac{32}{0.64g}$
解得:x=6.32g y=3.94g z=1.74g
剩余的高锰酸钾的质量为:10g-6.32g=3.68g;
(3)由上述计算可知,剩余固体中高锰酸钾的质量是3.68g,锰酸钾的质量为3.94g,二氧化锰的质量为1.74g.
答:(1)反应中出生成0.64g氧气;
(2)9.36g剩余物质中含有高锰酸钾、锰酸钾、二氧化锰;
(3)剩余固体中高锰酸钾的质量是3.68g等.
点评 此题考查的根据关化学方程式的计算,通过认真分析题干,直接得到氧气的质量,然后再求高锰酸钾锰酸钾、二氧化锰的质量,据此判断剩余固体中各物质的质量.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:计算题
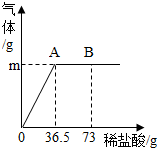 为测定某纯碱样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,
为测定某纯碱样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 粉身碎骨浑不怕,要留清白在人间 | B. | 欲渡黄河冰塞川,将登太行雪满山 | ||
| C. | 气蒸云梦泽,波撼岳阳城 | D. | 忽如一夜春风来,千树万树梨花开 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 元素的化学性质与原子的最外层电子数有关 | |
| B. | 原子核都是由质子和中子构成 | |
| C. | 金刚石和石墨物理性质有很大差异原因在于碳原子的排列方式不同 | |
| D. | 一氧化碳和二氧化碳的化学性质差异在于分子的构成不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室制氧气 2H2O=2H2O+O2↑ | |
| B. | 证明铜银的活动性 Cu+2 AgCl=2Ag+CuCl2 | |
| C. | 用赤铁矿石炼铁 Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | |
| D. | 钟乳石和石笋的形成 Ca(HCO3)2=CaCO3↓+CO2↑+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
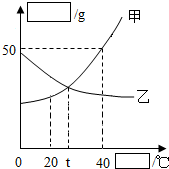 如图是甲、乙两种物质的溶解度曲线图:
如图是甲、乙两种物质的溶解度曲线图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com