

分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)
①实验室进行“过滤”操作使用的玻璃仪器主要有漏斗、烧杯和玻璃棒.由于加入的PbO2是过量的,所以过滤得到滤液I的同时得到的滤渣是剩余的PbO2,其化学式为PbO2.
②由于滤液I的主要溶质为Pb(NO3)2和NaC1O4,应该是NaClO3、PbO2、HNO3反应生成的Pb(NO3)2和NaC1O4,可能还有其他生成物,先假设该反应为NaClO3+PbO2+HNO3→Pb(NO3)2+?+NaC1O4.先简单配平为NaClO3+PbO2+2HNO3=Pb(NO3)2+?+NaC1O4.可知还缺少2个氢原子和1个氧原子,所以生成物还有水,对应的化学方程式为NaClO3+PbO2+2HNO3=Pb(NO3)2+H2O+NaC1O4.
③滤液I与KNO3发生反应制备KC1O4的,滤液I的主要溶质为Pb(NO3)2和NaC1O4,根据制备KC1O4可知,NaC1O4参与反应,所以是NaC1O4和KNO3反应生成KC1O4,则对应的化学方程式为NaClO4+KNO3=NaNO3+KC1O4(本题无法写出沉淀符号,只能是溶解度相对大小,可能在给定物质中KC1O4的溶解度最小而发生的反应).为两种化合物相互交换成分生成两种新的化合物,所以该反应为复分解反应.
(2)该转化关系应该首先读懂,290℃~370℃是PbO2会逐渐减少,到370℃是为零,而A物质从290℃到370℃逐渐增加,到370℃达到最大.而370℃~530℃,是A物质逐渐减少,而B物质逐渐增加.后续也是如此.
23.9 gPbO2,其中铅元素的质量为23.9g×$\frac{207}{207+16×2}$×100%=20.7g
①370℃时得到的A达到最多,A中含有的铅元素的质量为20.7g,而氧元素的质量为23.1g-20.7g=2.4g,则A中铅原子和氧原子个数比为$\frac{20.7g}{207}$:$\frac{2.4g}{16}$=2:3,所以A的化学式为 Pb2O3.530℃时得到的B达到最多,B中含有的铅元素的质量为20.7g,而氧元素的质量为22.83g-20.7g=2.13g,则A中铅原子和氧原子个数比为$\frac{20.7g}{207}$:$\frac{2.13g}{16}$=3:4,所以B 的化学式为 Pb3O4.
②若在某溫度下测得剩余固体的质量为22.94g,根据22.94g介于23.1g和22.83g之间,温度介于370℃~530℃之间,是Pb2O3逐渐分解生成Pb3O4的过程,所以有剩余的Pb2O3和生成的Pb3O4,所以此时得到的固体为Pb2O3和Pb3O4.
设混合物中Pb2O3的质量为x,则 Pb3O4的质量为22.94g-x.
由于过程中铅元素依旧为20.7g
则有$\frac{207×2}{207×2+16×3}$×100%×x+$\frac{207×3}{207×3+16×4}$×100%×(22.94g-x)=20.7g
x=9.52g
则 Pb3O4的质量为13.42g
所以 Pb2O3和Pb3O4的质量比为476:671(本题计算中保留有效数字影响最终计算结合,所以答案应该是大概范围).
故答案为:
(1)①玻璃棒; PbO2.
②NaClO3+PbO2+2HNO3=Pb(NO3)2+H2O+NaC1O4.
③NaClO4+KNO3=NaNO3+KC1O4; 复分解.
(2)①Pb2O3;Pb3O4.
②Pb2O3和Pb3O4; 476:671.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
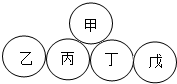
| A. | 丙是盐酸 | B. | 戊是氢氧化钙 | ||
| C. | 五种物质中,只有铁是单质 | D. | 甲与丁反应属于复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | pH大于7的溶液不一定是碱性溶液 | |
| B. | 不饱和溶液变为饱和溶液,溶质质量分数一定变大 | |
| C. | 向某固体中滴加稀盐酸,有气泡产生,则固体中一定含有碳酸根离子 | |
| D. | 金属与酸溶液发生置换反应,所得溶液质量一定大于原来酸溶液的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
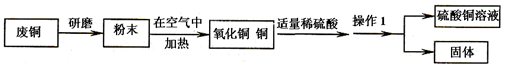
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com