
| A. | NaOH、NaCl、K2SO4 | B. | MgSO4、Cu(NO)3、KCl | ||
| C. | KNO3、ZnCl2、Ca(NO3)2 | D. | CaCl2、(NH4)2SO4、K2CO3 |
分析 pH为1的水溶液显酸性,水溶液中含有大量的H+.根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存;本题还要注意能得到无色溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为1的水溶液显酸性,水溶液中含有大量的H+.
A、H+和NaOH结合生成水,不能大量共存,故选项错误;
B、三者之间不反应,且能在酸性溶液中共存,但Cu(NO3)2溶于水呈蓝色,故选项错误;
C、三者之间不反应,能在酸性溶液中共存,且不存在有色离子,故选项正确;
D、Na2CO3中的碳酸根离子和和H+在溶液中能结合生成水和二氧化碳,和CaCl2结合产生碳酸钙沉淀,不能大量共存,故选项错误.
故选C.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意在酸性溶液中共存及特定离子的颜色.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
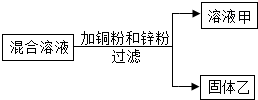 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
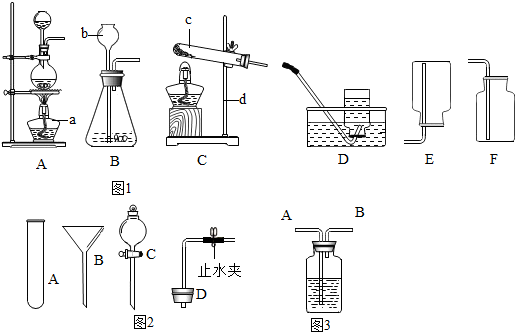
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

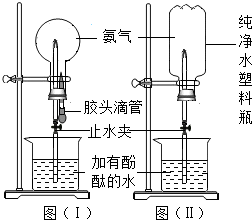
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
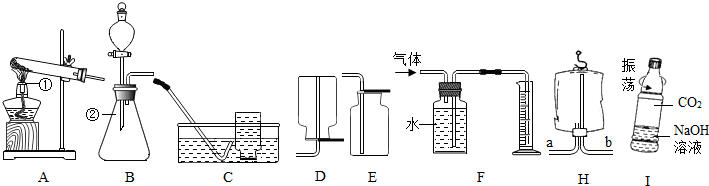
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
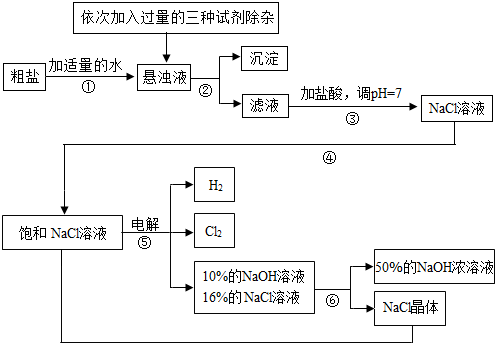
 某化学研究性学习小组,为除去粗盐中的Ca2+、Mg2+、Fe3+、$SO_4^{2-}$以及泥沙等杂质,设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
某化学研究性学习小组,为除去粗盐中的Ca2+、Mg2+、Fe3+、$SO_4^{2-}$以及泥沙等杂质,设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com