(2014?浦东新区一模)同学们对实验“煅烧石灰石”展开深入探究.
①煅烧石灰石.可观察到石灰石的表面
有气泡产生
有气泡产生
.
②为证明石灰石已分解,三位同学从其他角度设计方案如下:
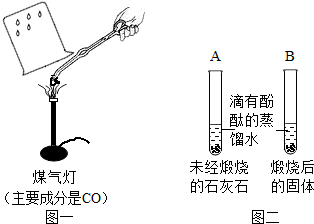
Ⅰ.甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式
Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
.
Ⅱ.乙同学按图二所示进行试验,观察到B中液体变
红
红
色,A中实验的作用
对照
对照
.
Ⅲ.丙同学取一块石灰石进行煅烧,一段时间后发现固体质量减轻mg(即CO
2的质量),证明石灰石已分解.
IV.大家认为甲同学的方案不合理,请分析原因
煤气灯的主要成分为一氧化碳,而一氧化碳燃烧生成了二氧化碳,所以澄清石灰水变浑浊不一定是来源于碳酸钙的分解
煤气灯的主要成分为一氧化碳,而一氧化碳燃烧生成了二氧化碳,所以澄清石灰水变浑浊不一定是来源于碳酸钙的分解
.
③为测定石灰石的纯度,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生mg气体,结合上述数据计算可知,丙所取的这块石灰石中含碳酸钙
mol(用m表示).

 (2014?浦东新区一模)同学们对实验“煅烧石灰石”展开深入探究.
(2014?浦东新区一模)同学们对实验“煅烧石灰石”展开深入探究.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案