
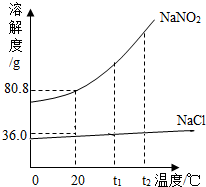
 已知:NaNO2(亚硝酸钠)的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃;NaNO2和NaCl的溶解度曲线如图所示.回答下列问题:
已知:NaNO2(亚硝酸钠)的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃;NaNO2和NaCl的溶解度曲线如图所示.回答下列问题:分析 (1)根据溶解度曲线可以判断溶解度的大小;
(2)溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
(3)根据溶解度可以进行相关方面的判断;
(4)根据物质的熔点不同可以进行区分.
解答 解:(1)t2℃时,NaNO2的溶解度更大;
(2)同温下,能够配制到相同溶质质量分数的NaNO2、NaCl的不饱和溶液;
(3)因为10mL水中能够完全溶解5.0gNaNO2,但是不能完全溶解5.0gNaCl,通过溶解情况可以区分NaNO2、NaCl;
(4)该方案可以是:把NaNO2和NaCl分别放在两个坩埚中同时加热,先熔化的是NaNO2,后熔化的是NaCl.
故填:NaNO2;能够;可行;10mL水中能够完全溶解5.0gNaNO2,但是不能完全溶解5.0gNaCl;把NaNO2和NaCl分别放在两个坩埚中同时加热,先熔化的是NaNO2,后熔化的是NaCl.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 馒头和稀饭 | B. | 鸡蛋和牛奶 | C. | 油条和豆浆 | D. | 炸鸡块和酸奶 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | La+HCl | B. | La2O3+HCl | C. | NaCl+La(NO3)3 | D. | La(OH)3+HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醇为无机物 | |
| B. | 甲醇由碳原子、氧原子、氢原子构成 | |
| C. | 甲醇中碳元素与氢元素的质量比为1:4 | |
| D. | 该合成过程CO和H2的质量比为7:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜粉和氧化铁粉末-稀硫酸 | B. | 稀盐酸和碳酸钠溶液-酚酞试液 | ||
| C. | 氯化钠粉末和硝酸铵粉末-水 | D. | 氮气和二氧化碳-燃着的木条 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com