
【题目】下图是“XX牌贴身暖宝宝”使用说明书,小王等同学阅读了使用说明后,对它的成分和发热原理产生了兴趣,和同学们一起进行了实验探究。
(1)【初步探究成分及发热原理】
【提出问题】“暖宝宝”为什么能发热?
【做出猜想】“暖宝宝”发出的热量主要来自铁粉氧化(即生锈)的过程。
【设计实验】
实验操作 | 实验现象 | 解释或结论 | |
步骤1 | 取A、B两袋“暖宝宝”,将A袋按使用说明打开外袋取出内袋;而B袋不打开外袋。并将两袋样品放置在同样的环境中。 | A袋的“暖宝宝”温度很快上升;B袋温度。 | “暖宝宝”发热是由于袋内物质与接触。 |
步骤2 | 24小时后,分别剪开A、B两袋,各取少量袋内物质于两支试管中,分别加入适量稀盐酸。 | A袋内物质部分溶解,产生黄色溶液;B袋内物质。 | 用化学方程式表示产生黄色溶液的反应 |
【得出结论】 “暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程。 | |||
【继续探究】小王和同学们想继续探究“暖宝宝”发热后,剩余物质中是否还含有活性炭,他们取适量A袋内物质于烧杯内,加入过量 , 充分反应后过滤,洗涤、干燥滤渣。
为进一步验证黑色滤渣的成分,小王和小李同学分别设计了甲、乙两个如图所示的装置,点燃滤渣,用澄清石灰水验证产物,你认为图的装置结论更可靠,理由是。
同学们分析铁生锈是一个缓慢氧化的过程,从原料角度分析“暖宝宝”放热现象之所以很明显是因为:
①铁呈粉末状,活性炭有吸附性,促使铁能与氧气、水等反应更快;②;
(2)【测定“暖宝宝”中的含铁量】
取一片包装完好的“暖宝宝”,剪开包装,利用袋内物质立即进行实验。
【实验方法】 取样品m g,利用如图丙所示装置与药品,测反应后生成气体的体积。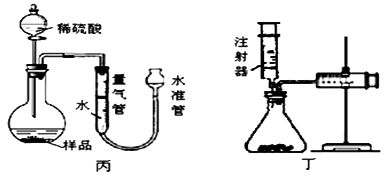
【实验步骤】① 连接仪器,;
② 将实验所用药品装入各仪器中,记录量气管初始刻度;
③ 打开分液漏斗活塞,加入足量稀硫酸至不再有气泡冒出。在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管(填“上提”或“下移”);
④ 等恢复至室温,并后,再次记录量气管刻度。
(3)【数据处理】
若实验条件下,氢气的密度为d g/mL,测得氢气体积为v mL。则该“暖宝宝”中铁粉的质量分数的表达式为。(用含dvm的字母表示)
(4)【交流讨论】利用丙装置,即使操作无失误,测量结果仍会偏大,原因是_,
小王重新设计了一个如图丁的实验装置,利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀硫酸体积为V1 mL,充分反应后,右侧针筒中气体变化的读数为V2 mL,则反应生成的氢气的体积为_ mL。
(5)【测定“暖宝宝”中的氧化铁的含量】
小李取了一片外袋已有部分破损的“暖宝宝”,剪开包装,取10g袋内物质立即进行实验。
【查阅资料】① 2Fe(OH)3 ![]() Fe2O3 + 3H2O ② Fe + 2 FeCl3 = 3 FeCl2
Fe2O3 + 3H2O ② Fe + 2 FeCl3 = 3 FeCl2
③ 在HCl和FeCl3的混合溶液中Fe先与FeCl3反应
【实验记录】
【实验结论】①写出产生气体的化学方程式___
②经该实验测定,该片已有破损的“暖宝宝”中的氧化铁的含量为 _ 。(写出计算过程)
【答案】
(1)无明显变化,O2 (或空气),部分溶解,有气泡产生,浅绿色溶液,Fe2O3+6HCl=2FeCl3+3H2O,稀盐酸或稀硫酸,甲,乙方案酒精燃烧生成的CO2会干扰实验,氯化钠能加快铁生锈
(2)检查装置气密性,下移,调节量气管与水准管两边液面相平
(3)![]() ×100%
×100%
(4)滴入烧瓶内的稀硫酸占一定体积,V2—V1
(5)Fe+2HCl=FeCl2+H2↑,16%
【解析】【设计实验】A袋中的物质与空气接触,只有铁常温能与氧气反应放出热量,生成铁锈(主要成分是Fe2O3),Fe2O3与稀盐酸反应生成氯化铁和水,氯化铁的溶液呈黄色,发生反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;B袋没有打开外袋,铁粉没有与氧气接触,不能发生缓慢氧化,故温度无明显变化,加入盐酸,铁与稀盐酸反应生成氯化亚铁和氢气,氯化亚铁的溶液呈浅绿色;
【继续探究】根据铁与盐酸反应,活性炭和盐酸不反应的原理,加入过量的稀盐酸除去铁粉;根据活性炭燃烧的产物是二氧化碳,可用澄清的石灰水检验二氧化碳的产生,乙图中酒精燃烧也会产生二氧化碳会干扰实验结果,故甲装置图得出的结论更可靠;①利用活性炭的吸附性可吸收空气中的氧气和水;②氯化钠也是促进铁粉生锈的因素之一,即氯化钠能加快铁生锈;①实验开始前必须先检查装置的气密性;③在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管下移,减小烧瓶和量气管内的压强;④根据连通器的原理可以知道,为了使实验结果准确,应该移动调节水准管和量气管中的液面相平后才能读数;【数据处理】
解:设铁粉的质量为X
Fe+2HCl=FeCl2+ | H2↑ |
56 | 2 |
x | dv |
![]() =
= ![]() , 解得:X=28dv
, 解得:X=28dv
铁的质量分数为: ![]() ×100%;
×100%;
【交流讨论】
丙装置加入的硫酸占据了一定的空间,使测得的气体的体积偏大,从而使得测定结果偏高;使用丁装置产生气体的体积应该等于注射器内气体的体积减去滴加的硫酸的体积,即反应生成的氢气的体积为V2—V1mL;
【实验结论】
混合物中的铁与稀盐酸反应生成氯化亚铁的同时得到氢气,发生反应的化学方程式为:Fe+2HCl=FeCl2+H2↑;
设生成0.2g氢气参加反应铁粉的质量为x
Fe+2HCl=FeCl2+ | H2↑ |
56 | 2 |
x | 0.2g |
则 ![]() =
= ![]() 解得:x=5.6g,
解得:x=5.6g,
根据反应流程可知碳粉的质量为1.9g,10.4g红棕色粉末为Fe2O3,则未氧化变质前Fe粉的质量为:10.4g× ![]() ×100%=7.28g,则剩余铁元素的质量为7.28g-5.6g=1.68g,这1.68g的铁元素发生了以下反应Fe+2FeCl3=3FeCl2,即铁单质与氯化铁中铁元素的质量比是1︰2,则参加反应铁单质的质量为1.68g×
×100%=7.28g,则剩余铁元素的质量为7.28g-5.6g=1.68g,这1.68g的铁元素发生了以下反应Fe+2FeCl3=3FeCl2,即铁单质与氯化铁中铁元素的质量比是1︰2,则参加反应铁单质的质量为1.68g× ![]() =0.56g,则破损的“暖宝宝”中的剩余铁单质的质量为5.6g+0.56g=6.16g;氧化铁中铁元素的质量为7.28g-6.16g=1.12g,则对应氧化铁的质量为1.12g÷(
=0.56g,则破损的“暖宝宝”中的剩余铁单质的质量为5.6g+0.56g=6.16g;氧化铁中铁元素的质量为7.28g-6.16g=1.12g,则对应氧化铁的质量为1.12g÷( ![]() ×100%)=1.6g,故该片已有破损的“暖宝宝”中的氧化铁的含量为
×100%)=1.6g,故该片已有破损的“暖宝宝”中的氧化铁的含量为 ![]() =16%。
=16%。
所以答案是:无明显变化;O2 (或空气);部分溶解,有气泡产生,浅绿色溶液;Fe2O3+6HCl=2FeCl3+3H2O;稀盐酸或稀硫酸;甲;乙方案酒精燃烧生成的CO2会干扰实验;氯化钠能加快铁生锈;检查装置气密性;下移;调节量气管与水准管两边液面相平;![]() ;滴入烧瓶内的稀硫酸占一定体积;V2—V1;Fe+2HCl=FeCl2+H2↑;16%。
;滴入烧瓶内的稀硫酸占一定体积;V2—V1;Fe+2HCl=FeCl2+H2↑;16%。


科目:初中化学 来源: 题型:
【题目】下列成语与对应的燃烧或灭火原理不相符的是( )
A.钻木取火一一使可燃物达到着火点
B.釜底抽薪——清除可燃物
C.火上浇油——隔绝空气
D.煽风点火——增大氧气含量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.根据质量守恒定律,1L氢气和1L氧气反应能生成2L水
B.蜡烛完全燃烧后,蜡烛没有了,这违背了质量守恒定律
C.只有固体、液体间反应遵守质量守恒定律
D.铁在氧气中燃烧,生成四氧化三铁的质量等于参加反应的铁丝与氧气的质量之和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】著名科学家居里夫人首先发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。一种元素的原子经过放射变成另一种元素的原子,据此推断放射出的粒子一定是( )
A.离子B.质子C.中子D.原子核
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有①水 ②液氧 ③高锰酸钾 ④四氧化三铁 ⑤海水⑥过氧化氢溶液六种物质,其中属于混合物的有___________,属于氧化物的有___________,属于单质的有____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某大理石样品(杂质不溶于水也不与稀盐酸反应)中碳酸钙的含量,某中学化学兴趣小组的同学取12g样品放人烧杯中,加入100g稀盐酸,恰好完全反应,称得反应后烧杯中剩余物质的总质量为107.6g(产生的气体全部逸出)。试计算:
(1)反应生成二氧化碳的质量是多少克?
(2)大理石样品中碳酸钙的质量分数。(计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有以下物质:A二氧化硫 B稀有气体 C一氧化碳 D干冰,请按要求填空(填字母,不重复)。
(1)通常用于冶炼金属的是_______________。
(2)可作灯泡填充气的是_______________。
(3)用于冷藏保存食品的是_______________。
(4)形成酸雨的污染物是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关说法不正确的是
A.氯化钠溶于水是因为氯化钠分子不断运动
B.水受热变为水蒸气体积变大是因为分子间隔变大
C.CO与CO2化学性质不同是因为构成它们的分子不同
D.氢气燃烧过程中改变的是氢分子和氧分子,氢原子和氧原子不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com