
 Ϊ����ij������ͭ��ͭ��ɵĻ����������ͭ����������ȡ3�ݸû�����20g���ֱ������뵽50g��100g��150gijϡ�����У��������ʵ���������±���
Ϊ����ij������ͭ��ͭ��ɵĻ����������ͭ����������ȡ3�ݸû�����20g���ֱ������뵽50g��100g��150gijϡ�����У��������ʵ���������±���| ��� | A | B | C |
| ϡ���������/g | 50 | 100 | 150 |
| ʣ����������/g | 10.0 | 16.0 | 16.0 |
���� ����Ʒ�е�����ͭ�����ᷴӦ��ͭ�������ᷴӦ����A��ʵ��50gϡ����ʣ������������10.0g����B��ʵ����100gϡ����ʣ������������16.0g����C��ʵ����150gϡ����ʣ������������16.0g���ɴ˵ó����ۣ���A��ʵ����㣬����ͭ��ʣ�࣬��BC��ʵ����ʣ������ͭ��ȫ��Ӧ����
��� �⣺��1����Ʒ�е�����ͭ�����ᷴӦ��ͭ�������ᷴӦ����A��ʵ��50gϡ����ʣ������������10.0g����B��ʵ����100gϡ����ʣ������������16.0g����C��ʵ����150gϡ����ʣ������������16.0g���ɴ˵ó����ۣ���A��ʵ����㣬����ͭ��ʣ�࣬��BC��ʵ����ʣ������ͭ��ȫ��Ӧ����
��2����Ʒ�е�����ͭ�����ᷴӦ��ͭ�������ᷴӦ�����Ե�BC��ʵ����ʣ������ͭ��ȫ��Ӧ����ʣ����������16g����Ϊ20g�û������Ʒ�к�����ͭ��������
��3���������������������Ϊx
CuO+H2SO4�TCuSO4+H2O
80 98
10g 50g��x
$\frac{80}{10g}=\frac{98}{50g��x}$
x=24.5%
������ϡ�����������������Ϊ24.5%��
��4�����16g����ͭ��Ӧ��ϡ��������Ϊy�����ɵ�����ͭ������Ϊz��
CuO+H2SO4�TCuSO4+H2O
80 98 160
16g 24.5%��y z
$\frac{80}{16g}=\frac{98}{24.5%��y}=\frac{160}{z}$
��� y=80g
��� z=32g
��ͣ�100g-80g��ϡ���ᷴӦ������������Һ������Ϊm��
H2SO4+2NaOH=Na2SO4+2 H2O
98 80
��100g-80g����24.5% 10%��m
$\frac{98}{��100g-80g����24.5%}=\frac{80}{10%��m}$
���m=40g
��Ϊ����ϡ���������ͭ����Һ�еμ�����������Һʱ�����Կ�������������Һ�Ⱥ����ᷴӦ�ٺ�����ͭ��Ӧ���������ǵõ�������꣨40��0����
������ɵ�����ͭ��Ӧ������������Һ������Ϊn����Ӧ���ɵij���������Ϊw��
CuSO4+2NaOH=Cu��OH��2��+Na2SO4
160 80 98
32g 10%��n w
$\frac{160}{32g}=\frac{80}{10%��n}=\frac{98}{w}$
���n=160g��w=19.6g
��ʣ���ϡ�����Լ�����ͭ��Ӧ������������Һ�������ܺ���40g+160g=200g���������ǵõ��۵����꣨200��19.6�����ʻ���ͼ����ͼ��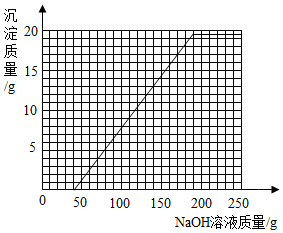
�ʴ�Ϊ����1��A����2��16��
��3��24.5%����4�� ��
��
���� ��������ͼ���ķ�ʽ�������ͽ����ѧ�����е��й����⣬Ҫ��ѧ���н�ǿ��ʶͼ���������ݷ��������Լ�����ͼ���������


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ | B�� | ��ɫ | C�� | ��ɫ | D�� | ���ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��֪A��BΪ���ֺ�ɫ��ĩ��DΪ��ɫ���ʣ�A��B��C��D��E��F��������֮���ת����ϵ��ͼ��ʾ����������������ʡ�ԣ���ش�
��֪A��BΪ���ֺ�ɫ��ĩ��DΪ��ɫ���ʣ�A��B��C��D��E��F��������֮���ת����ϵ��ͼ��ʾ����������������ʡ�ԣ���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �¶�/�� | 0 | 20 | 40 | 60 | 80 |
| �ܽ��/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
| A�� | ��20��ʱ����100 gˮ�м���40 g����ع��壬�ܹ��õ�140 g��Һ | |
| B�� | ������Һ�¶Ȳ������ߣ�����ع�����ܽ�ȳ��ֳ����ϼ��ٵ����� | |
| C�� | 60��ʱ210 g����ر�����Һ���µ�20�棬������78.4 g����ؾ��� | |
| D�� | ��40��ʱ����صı�����Һ�м��������Ȼ��ƹ��壬�Ȼ��Ʋ����ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
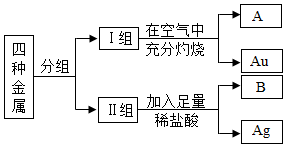 ij����С���ͬѧ����ʦ�İ����´ӷ����ҵ��л��������Fe����ͭ��Cu��������Ag������Au�����ֽ�����������������ֽ����أ�ͬѧ�ǽ�������ʵ�飺
ij����С���ͬѧ����ʦ�İ����´ӷ����ҵ��л��������Fe����ͭ��Cu��������Ag������Au�����ֽ�����������������ֽ����أ�ͬѧ�ǽ�������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

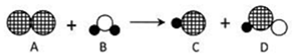
 �������𡱡���������ͬԭ�ӣ�����DΪ�����ᣨHClO������ɱ���������ã�Һ����ˮ��Ӧ�Ļ�ѧ����ʽ��Cl2+H2O=HCl+HClO��
�������𡱡���������ͬԭ�ӣ�����DΪ�����ᣨHClO������ɱ���������ã�Һ����ˮ��Ӧ�Ļ�ѧ����ʽ��Cl2+H2O=HCl+HClO���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
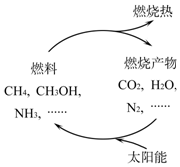 ��ѧ������Ƽ�������������أ�
��ѧ������Ƽ�������������أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�����ʵļ��� | B�����ʵij��� |
| ���壨�������ơ��Ȼ��ƣ�--ˮ ��Һ���������ơ����ᣩ--��̪��Һ | �Ȼ����л�����������ͭ����--�������� CO2��������CO����--��ȼ |
| C�����ʵ���; | D�����ʵķ��� |
| С�մ�̼���--����θ����� �ռ��ʯ��--������������ | ������--���� ����п����Ԫ��--����������Ԫ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2 | B�� | N2 | C�� | CO2 | D�� | CO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com