

| ||
| ||
| ||
| ||


 学习实践园地系列答案
学习实践园地系列答案科目:初中化学 来源: 题型:
| 实验编号 | a | b | cw | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
查看答案和解析>>
科目:初中化学 来源: 题型:
A、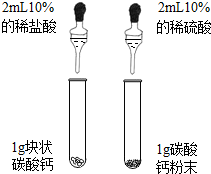 探究反应物接触面积对反应速率的影响 探究反应物接触面积对反应速率的影响 |
B、 探究二氧化碳能与水发生反应 探究二氧化碳能与水发生反应 |
C、 探究反应物浓度对反应速率的影响 探究反应物浓度对反应速率的影响 |
D、 探究燃烧的温度是否须达到着火点(白磷着火点:40℃) 探究燃烧的温度是否须达到着火点(白磷着火点:40℃) |
查看答案和解析>>
科目:初中化学 来源: 题型:
| OH- | SO42- | |
| Zn2+ | 不 | 溶 |
| Fe2+ | 不 | 溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com