
����Ŀ�����������౦�����Ȼ��Դ����ˮ���Ƽ�����˻�ѧ��ѧ�ڸ��������е��ǻۣ�
��ͼ��ij����������Ĺ�������ͼ��

������������⣺
��1����������Ϊ�˳�ȥ���ʣ��������BaCl2��Һ��NaOH��Һ��Na2CO3��Һ������˵����ȷ����______________________������ĸ��ţ���
A.����������Һ��˳���ܵ���
B.����������Һ������ˮ�е�SO42����Mg2+��Ca2+ת��Ϊ����
C.��������������Һ��˳����ӣ����˺�õ����ֳ���
��2�����������У�����BaCl2��Һʱ������Ӧ�Ļ�ѧ����ʽ��______________________��
��3�����������У�������백������Ϊ�������Ȼ������������Ƽ�����е�������__��
��4��д���������з�����Ӧ�Ļ�ѧ����ʽ____________________________��
���𰸡���1��̼���ƺ��Ȼ�李���2��BC
��3�������Ӷ�����̼������
��4��2NaHCO3��Na2CO3+H2O+CO2��
�������������������1��������������̼�����ƺ��Ȼ�泥��Ȼ�刺������ʡ�̼������������III�л�����̼���ơ����Ըó����յIJ�Ʒ��̼���ƺ��Ȼ�李�
��2�������Ȼ���������������ӽ���γ����ᱵ��������������������Ϊ�˳�ȥþ���ӣ�����̼������Ϊ�˳�ȥ�����ӡ�����B����ȷ��Ϊ����ȫ��ȥ��������ӣ�������Ҫ����������Ȼ��������������ж�����Ҫ�ù����ı������γɳ������������̼���Ƽ����뱵���ӽ���γ�̼�ᱵ����������ͼʾ�����˳�������ֳ�����C����ȷ����������������֪����̼����һ��Ҫ�ڼ����Ȼ���֮������˳����Ե���������A���ȷ������ӦѡBC�
��3�����Ȼ���ת��Ϊ̼������Ҫ�γ�̼���������Ӧ���մ����Ķ�����̼����������ˮ��Һ�ʼ��ԣ������Ӷ�����̼��������
��4������III�У�̼�������ڼ��ȵ����������̼���ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3��Na2CO3+H2O+CO2��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ�����˵����ȷ���ǣ� ��
A.����ʹ�ý��������������ͭ����
B.������»�������������Au���ڸ���������Ҳ������������Ӧ
C.ͨ����¯���õ���Ϊ����
D.��ºϽ���۵�ߣ����������챣��˿
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼��ƹ㷺Ӧ���������ϡ����ᡢˮ��Ϳ���Լ���ֽ����ҵ���ճ������е�����Ҳ��������Ħ������Ŀǰ����̼��Ƶ�������Ҫ��̼�������������̼���ͼ��
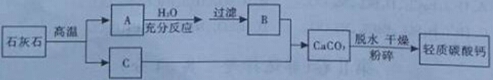
���������̼��Ƶ��������̣��ش��������⣺
��1������B�Ļ�ѧʽΪ ��
��2����A��B֮�䣬���˲�����Ŀ���� ��
��3����B+C��CaCO3�Ĺ����У�Ӧ��������C��������ԭ���� ���û�ѧ����ʽ��ʾ����
��4����������̼��Ƶķ����ܶ��������һ���Ʊ����� ���û�ѧ����ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʣ��������ŷŵ�β������úȼ�ղ������̳����ۻ������ŷų��ķ������ܽ��Ӻ� ����������ˮ��������ֲ�������÷ų������壻���˺����Ķ�����̼��������������Ⱦ��������������ɺܴ�Σ���������� ( )
A. �٢ۢ� B. �ڢܢ� C. �٢ڢ� D. �ܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50ml�ƾ���50mlˮ��Ϻ�����_______(������������<������>��)100ml��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ȡ��ҩƷʱ�����û��������Һ��ȡ_______������ֻ��____________������Ͳ��ȡҺ��ʱ��Ͳ�����_____������ʹ��������Ͳ��Һ��________________����ˮƽ���ٶ�����ȡҺ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���淶�IJ�����ʵ��ɹ��ı�֤������ʵ�������ȷ����
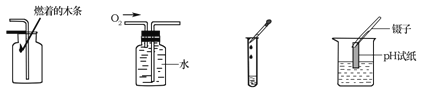
A��CO2���� B���ռ�O2 C���μ�Һ�� D������ҺpH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����6�֣������ᣨHClO4�����������ƣ�NaClO2���ڹ�ҵ���й㷺����;�����Ʊ������������£�
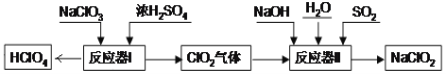
��ش��������⣺
��1��HClO4��ClԪ�صĻ��ϼ��� ��
��2����Ӧ��I�е���������HClO4��ClO2��NaHSO4��H2O������������������� ��
��3����Ӧ��II�з�����Ӧ�Ļ�ѧ����ʽΪ2ClO2+SO2+4NaOH=2NaClO2+X+2H2O����X�Ļ�ѧʽ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com