
(8分) (1)用数字和化学符号表示:
①2个氧原子 ;② 氯化钠中的阳离子 ;③氧化镁中镁元素化合价为+2 ;
(2) 请将下列物质按照一定的要求从大到小(由高到低、由多到少)排列(填序号)。
Ⅰ.相对分子质量:①二氧化碳 ②氢气 ③氮气____________________
Ⅱ.每个分子中的原子个数:①水 ②氨气 ③氧气_________________
Ⅲ.地壳中元素含量:①O ②Al ③Si _____________________
(3)下列物质:①河水 ②镁条 ③ 冰水 ④液氧 ⑤五氧化二磷 ⑥锰酸钾 ⑦人体呼出的气体 ⑧5%的过氧化氢溶液 ⑨铜绿完全分解后的剩余固体
属于单质的是(填化学式,下同)_____ _____;属于氧化物的是___ ____。
(1) ① 2O ; ② Na+;③ MgO ;
(2) 从大到小(由高到低、由多到少)排列(填序号)。
Ⅰ.132 Ⅱ.213 Ⅲ.132
(3)Mg.、O2; H2O 、 P2O5 、CuO。
【解析】
试题分析:(1)①2个氧原子:2O;② 氯化钠中的阳离子:Na+;③氧化镁中镁元素化合价为+2: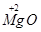 ;
;
(2)Ⅰ.相对分子质量由大到小:①二氧化碳、③氮气、②氢气;
Ⅱ.每个分子中的原子个数由多到少:②氨气、①水、③氧气;
Ⅲ.地壳中元素含量由高到低:①O 、③Si、②Al 。
(3)题中物质中属于单质的是Mg.、O2;属于氧化物的是H2O 、 P2O5 、CuO。
考点:化学符号;相对分子质量;原子个数;地壳中元素的含量;单质;氧化物。
点评:元素用元素符号表示;原子用元素符号表示,若表示原子个数,就在元素符号前标上适当的数字;分子用化学式表示,表示分子的个数,就在化学式前加上适当数字表示;离子则在元素符号右上角标上适当的电荷数就行了,化合价标注在元素符号的正上方。
地壳中元素含量的多少顺序为:氧、硅、铝、铁、钙、钠、钾、镁;
相同质量的气体,相对分子质量越小的,其中包含的气体分子数越多。


科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 使用现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 | 现象一与现象二对比,说明 ① ▲ |
| 现象二:粗砂纸打磨的片刻内现象不明显。 | ||
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 | 现象三与现象一对比,说明 ② ▲ |
| 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象四与现象三对比,说明 ③ ▲ |

查看答案和解析>>
科目:初中化学 来源:2013届北京市海淀区九年级上学期期中考试化学试卷(带解析) 题型:探究题
(8分)在对蜡烛及其燃烧的探究实验中,小明仔细观察蜡烛燃烧时的火焰,发现火焰中不同区域的明亮程度不同,这是为什么呢?在老师的指导下小明进行了以下探究活动。
【查阅资料】
(1)可燃物的种类及组成会影响火焰的明亮程度。
(2)蜡烛主要由石蜡制成,石蜡是石油炼制后得到的固体物质,主要由多种碳氢化合物组成,这些化合物分子中的碳原子数目不唯一,其化学式通式为CnH2n+2 ,通式中碳原子数n = 18~30。
(3)碳氢化合物在常温时的状态如下表所示。
| 物质名称 | 化学式 | 常温时的状态 |
| 丁烷 | C4H10 | 气 |
| 戊烷 | C5H12 | 液(油状) |
| 癸烷 | C10H22 | 液(油状) |
| 十八烷 | C18H38 | 固 |
| 二十四烷 | C24H50 | 固 |
| 序号 | 实验目的 | 实验操作 | 实验现象 |
| I | 探究哪一层火焰的温度最高 | 点燃蜡烛,把一根火柴梗平放在蜡烛的火焰中,约1s后取出观察 | |
| Ⅱ | 探究焰心中参与燃烧的物质的成分 | 点燃一根较粗的蜡烛,取一根一端为尖嘴的玻璃导管,一端伸入火焰的焰心处,然后在尖嘴一端导管口用火柴点燃 | 导管口处出现火焰 |
| III | 继续探究焰心中参与燃烧的物质的成分 | 点燃一根蜡烛,用一把带有手柄的小刀,将刀尖伸入火焰中最暗的部分,即焰心处,一段时间后取出,冷却,观察刀尖处的现象 | 冷却至室温后,刀尖处有油状液体和固体物质 |
| IV | | 用镊子夹住一片白瓷片,将瓷片伸入火焰中最明亮的部分,即内焰处,观察现象 | 白瓷片表面迅速变黑 |
查看答案和解析>>
科目:初中化学 来源:2011届广东省清远市初中毕业生学业考试化学试卷 题型:填空题
(8分)2011年3月11日,日本发生9.0级大地震,导致日本福岛第一核电站发生核辐射泄漏。
(1)福岛核电站机组反应堆芯发生核反应放出的氢气,接触外界的氧气发生剧烈反应,导致连续爆炸。请写出氢气爆炸时的化学方程式为 。
(2)我国政府向日本提供了人道主义援助,援助的物质包括:一次性防护服,活性炭防护口罩,骨科内外固定材料,饮用水等等。其中防护口罩主要利用了活性炭的 性。(3)由于堆芯熔毁,造成用来冷却反应堆的海水遭到反应堆内发生核裂变产生的放射性碘-131和铯-137的污染。由于运输困难和水资源遭到污染造成数百万人饮水困难。
① 生活中既能降低水的硬度,又能杀菌消毒的方法是 _______________;
②“水是生命之源”。下列关于水的说法正确的是_______。
A.水是单质,能赋予生命
B.水是一种很好的溶剂,能维持人体的体液平衡
C.水资源紧缺既有缺水又有水受到污染的原因,所以既要节约用水又要防止水污染
D.水中氧元素含量很高,能提供人体所需的氧气
(4)这次因冷却故障导致核反应堆发生爆炸,为中国核电站的快速扩张和核安全敲响了警钟,应该思考如何和平、安全利用原子能。下列说法中正确的是 。
A.核能的利用证实原子的可分性
B.核能的危害性太大,不应再推广使用
C.开发核能可节约化石能源
查看答案和解析>>
科目:初中化学 来源:2010-2011学年北京市海淀区中考一模化学试卷(解析版) 题型:填空题
(6分)2011年3月,日本海啸引发福岛第一核电站的放射性物质外泄,有关131I(碘-131)的相关报道成为热门话题。请回答下列问题:
(1)碘元素在体内发挥重要作用,但过量补碘也会引起甲亢等疾病。目前我国各地检测出的131I含量很小,根据京津等地检出的数值,吃上2000 kg的菠菜才相当于照一张X光片的辐射量。根据以上资料分析,下列说法正确的是____________。
a.盲目服用碘片等预防辐射对身体可能造成负面作用
b.我们应尽可能主动多摄入含碘食品,多多益善
c.以目前我国检测出的131I含量来看,对身体健康影响很小,不必恐慌
(2)131I原子中含有53个质子,78个中子。
①131I原子的核外电子数为__________。
②自然界中普遍存在另一种稳定的碘原子127I,它和131I同属于碘元素。127I原子的质子数为__________。
(3)专家指出,服用碘片(有效成分为KI)可以治疗131I造成的辐射,但服用碘酒(有效成分为I2)却会引起碘中毒。KI和I2性质的不同的原因是_________。
(4)①食盐中常添加碘酸钾(KIO3)以补充碘元素。已知KIO3中钾元素的化合价为+1,其中碘元素的化合价为__________。
②服用碘片治疗131I辐射的推荐服用剂量是每日摄入KI为130-170 mg,假设服用某碘片每日补充166 mg KI。已知每千克某品牌碘盐中KIO3的加入量为42.8 mg,如果用该食盐替代碘片提供治疗辐射所需的碘元素,则每日需食用该食盐的质量为__________kg。
查看答案和解析>>
科目:初中化学 来源:2011年初中毕业升学考试(福建厦门卷)化学 题型:填空题
(8分)碘元素是人体必需的微量元素之一。

(1)右图是元素周期表中碘元素的部分信息。碘原子的核电荷数是 ,碘元素属于 (填“金属”或“非金属”)元素。
(2)已知某碘盐的主要成分为氯化钠和碘酸钾(KIO3):
①氯化钠含有的阴离子是 (用符号表示),KIO3中I的化合价为 。
②用试剂X测定该碘盐中碘元素的含量,发生如下反应:
KIO3 + 5 X + 3H2SO4 = 3K2SO4 + 3 I2 + 3H2O,推算X的化学式为 。
③已知每包碘盐中最多含碘元素15 mg,则每包碘盐中最多含KIO3的质量为
mg(列出计算式即可,碘的相对原子质量从上图中查找)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com