
【题目】下列关于①~④所得溶液的说法正确的是
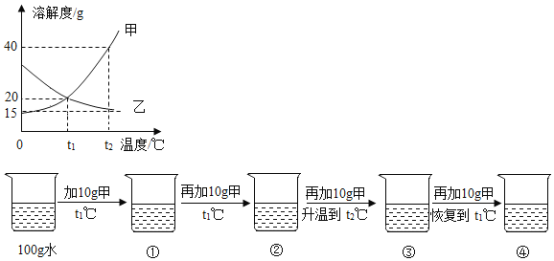
A.溶质质量:①=②
B.③中溶质与溶剂的质量比为1:2
C.溶液质量:③>④
D.④中溶质的质量分数约为33.3%
【答案】C
【解析】
A. t1℃时,甲溶解度为20g,则①中溶质质量为10g,②中溶质质量为20g,溶质质量:①≠②,说法错误;
B. 甲溶解度随温度升高而增大,②中恰好为t1℃下甲的饱和溶液,溶质质量为20g,溶剂质量为100g,再加入10g甲、温度升高至t2℃得到③,t2℃时,甲溶解度为40g,③中溶质质量为30g、溶剂质量为100g,③中溶质与溶剂的质量比为30g:100g=3:10,说法错误;
C. ③中溶质质量为30g,④中溶质质量为20g,溶液质量:③>④,说法正确;
D. 因温度恢复到t1℃,甲晶体析出,溶质质量重新变为20g,④中溶质的质量分数为![]() ,说法错误。
,说法错误。
故选:C。


科目:初中化学 来源: 题型:
【题目】某种天然碱样品的化学式可以用xNaHCO3·yNa2CO3·zH2O表示(式中x、y、z是 最简整数比)。取50g某一浓度的盐酸与3.32g样品充分反应,能生成1.32gCO2气体。
(1)若改用1.66g样品与50g这种盐酸反应,能产生 gCO2。
(2)另取3.32g样品在300℃下加热至完全分解(已知:![]() , Na2CO3在300℃时不会分解),能产生0.22gCO2和0.45gH2O,试确定该样品的化学式: 。
, Na2CO3在300℃时不会分解),能产生0.22gCO2和0.45gH2O,试确定该样品的化学式: 。
(3)写出这种天然碱与盐酸完全反应的化学方程式。若6.64g天然碱样品与50g该盐酸能恰好完全反应放出,求该盐酸的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。分析并计算:
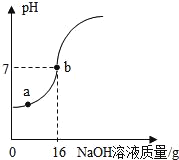
(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。_____
(4)计算恰好完全反应时所得溶液的溶质质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。请从两个方案中任选1个作答,若两个均作答,按方案A计分。
方案A | 方案B |
|
|
(1)实验中发生反应的化学方程式为______。 (2)实验中观察到的现象是______。 (3)该方案______(填“能”或“不能”)验证三种金属的活动性。 | (1)实验中发生反应的化学方程式为______。 (2)实验中观察到的现象是______。 (3)该方案______(填“能”或“不能”)验证三种金属的活动性。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】立德粉(ZnS·BaSO4)是一种常用白色颜料,以重晶石(BaSO4)为原料生产立德粉的主要工艺流程如下:
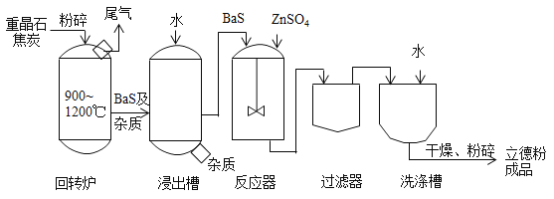
资料:BaS可溶于水,ZnS和BaSO4均难溶于水。
(1)回转炉中,重晶石(BaSO4)与焦炭在高温下焙烧制得BaS,其中一个化学反应为BaSO4+ 2C![]() 2CO2↑+ BaS,这个反应中,化合价发生变化的元素有______。
2CO2↑+ BaS,这个反应中,化合价发生变化的元素有______。
(2)反应器中发生复分解反应的化学方程式为______。
(3)上述流程中,主要用于分离、提纯的设备有______、过滤器和洗涤槽。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究反应物浓度对硫代硫酸钠(Na2S2O3)与硫酸反应速率的影响。
(查阅资料)
a Na2S2O3易溶于水,能与硫酸发生反应:![]()
b 浊度计用于测量浑浊度。产生的沉淀越多,浑浊度(单位为NTU)值越大。
(实验过程)
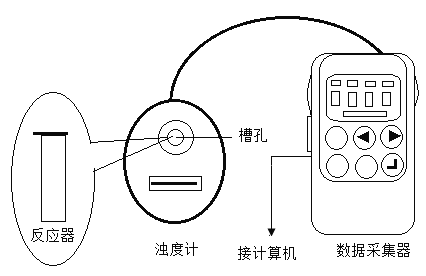
20℃时,用图所示装置进行如下表所示的5个实验,分别测量混合后溶液达到相同浑浊度的过程中,浑浊度随时间的变化。实验①~⑤所得数据如图所示。
实验编号 | 1.6% Na2S2O3溶液体积/ mL | 1% H2SO4溶液体积/ mL | 水体积/ mL |
① | 1.5 | 3.5 | 10 |
② | 2.5 | 3.5 | 9 |
③ | 3.5 | 3.5 | x |
④ | 3.5 | 2.5 | 9 |
⑤ | 3.5 | 1.5 | 10 |
注:所用溶液的密度均按1 g/mL计。
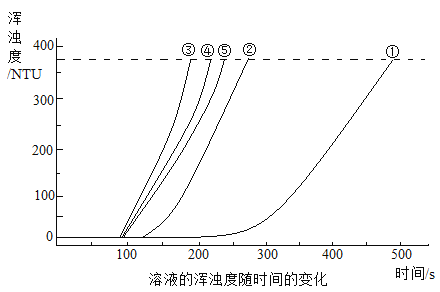
(解释与结论)
(1)选用浊度计进行测量,原因是Na2S2O3溶液与H2SO4溶液反应生成了_______。
(2)实验①~⑤中,反应速率最快的是_______(填实验编号)。
(3)实验③中,x=_______。
(4)实验①、②、③的目的是_______。
(5)比较①、②、③与③、④、⑤两组实验,可推断:改变_______(填“A”或“B”)对Na2S2O3与硫酸反应速率的影响更大。
A Na2S2O3溶液浓度
B H2SO4溶液浓度
你推断的证据是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】世界上每年因锈蚀而损失大量铁制品。某化学小组设计如下实验,探究铁生锈的条件及影响生锈速率的因素。

(进行实验)
实验1:分别取铁钉按下图装置所示,放置一周,结果如下:
序号 | 1-1 | 1-2 | 1-3 |
实验 |
|
|
|
现象 | 无明显现象 | 无明显现象 | 铁钉表面有红色固体 |
实验2:分别取铁钉浸于等体积的不同试剂中,放置一周,结果如下:
| 序号 | 2-1 | 2-2 | 2-3 |
试剂种类 | 蒸馏水 | 3%的NaCl溶液 | 3%的稀盐酸 | |
U形管左侧液面 | 上升1.2cm | 上升3.7cm | 上升5.3cm |
(解释与结论)
(1)铁生锈属于_______(填“物理”或“化学”)变化。
(2)铁锈中含有Fe、O、H元素,从元素守恒角度说明理由:_____________。
(3)实验 1 中,证明铁生锈需要与水接触的现象是___________。
(4)实验2-1中,U形管左侧液面上升的原因是__________。
(5)实验2的目的是_________。
(反思与评价)
(6)结合本实验,对于铁制品的保存,你的建议是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组想测定某铁合金中铁的含量,做了如下实验,称取14克样品,放入质量为50克的烧杯中,再往烧杯中加入100克足量的稀硫酸(杂质碳不与酸反应,也不溶于水),
并对烧杯进行了四次称量,记录数据如下:
反应时间 | T0 | T1 | T2 | T3 |
烧杯总质量(克) | 164 | 163.8 | 163.6 | 163.6 |
求(1)反应产生的氢气的质量是多少?
(2)该样品中铁的质量分数是多少?
(3)反应后所得溶液中溶质质量分数是多少?(要求写出计算过程,结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
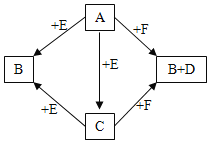
【题目】A、B、C、D、E、F是初中化学常见的物质,它们有如图所示的转化关系(→表示反应一步完成,反应条件略)。已知A、D、E是单质,F为红色固体,B、C是组成元素完全相同的两种气体。
(1)E物质的名称为_____。
(2)物质B在生产或生活中的一种用途是_____。
(3)反应C+F的化学方程式为:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com