
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | HCl(CO2) | 适量NaOH溶液 | 洗气 |
| B | NaCl(NaOH) | 过量稀盐酸 | 蒸发结晶 |
| C | CO2(CO) | 足量O2 | 点燃 |
| D | CaO固体(CaCO3) | 足量的水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、NaOH能与过量盐酸反应生成氯化钠和水,再蒸发结晶除去过量的盐酸和水分,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
D、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 磷烯是与硅一样的半导体,可用于制作太阳能电池 | |
| B. | 原子、原子核、夸克、质子时按空间尺度从大到小排列的 | |
| C. | 电荷磁的性质有许多相似之处,如同种电荷相互排斥,同名磁极相互排斥 | |
| D. | 汉中油菜花节上,游客远远地就能闻到花的香味,说明分子做无规则运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
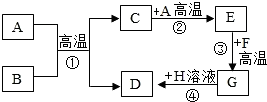 A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐,它们之间的转化关系如图所示,请回答:
A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐,它们之间的转化关系如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 科学家最近研制出一种以锶做钟摆的钟,它是世界上最精确的钟,锶在元素周期表中的某些信息如图所示,下列说法正确的是( )
科学家最近研制出一种以锶做钟摆的钟,它是世界上最精确的钟,锶在元素周期表中的某些信息如图所示,下列说法正确的是( )| A. | 锶属于非金属元素 | B. | 锶的中子为数为38 | ||
| C. | 锶的相对原子质量为87.62g | D. | 锶原子核外电子数为38 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间/S | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加质量/g | 0 | 0.7 | 1.0 | m | 1.5 | 1.6 | 1.7 | 1.7 |
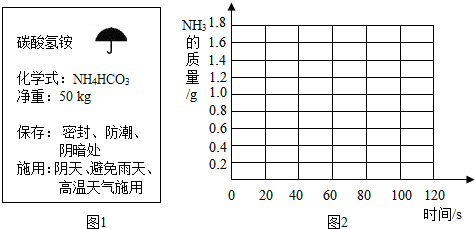
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成黑色固体 | |
| B. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| C. | 点燃羊毛纤维时能闻到烧焦羽毛的气味 | |
| D. | 向氢氧化钠溶液中滴入几滴无色酚酞溶液,溶液由无色变蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验装置 | 实验现象 | 实验结论 |
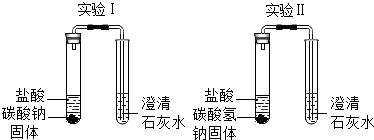 | 实验Ⅰ、Ⅱ中均观察到:白色固体逐渐减少,有气泡产生;澄清石灰水变浑浊 | Na2CO3和NaHCO3都能与盐酸反应产生CO2;NaHCO3与盐酸反应的化学方程式是NaHCO3+HCl═NaCl+H2O+CO2↑ |
| t1/℃ | t2/℃ | t3/℃ | |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅰ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 | 澄清石灰水无明显变化 |
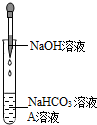
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com