某研究性学习小组在学习金属铁的知识后,为了解铜及其常见化合物的性质,运用类比的思想提出了如下问题,并进行探究.请帮助完成下列有关研究并填写有关空白.
【提出问题】
①铁能与稀硫酸反应产生氢气,铜能吗?铜与浓硫酸会发生反应吗?
②铁在潮湿的空气中易生锈,铜“生锈”需要什么条件?
③氧化铜能够被一氧化碳还原,也能被NH
3、CH
4还原吗?氧化铜还有哪些性质?
④氧化铜能直接转化为氢氧化铜吗?有哪些途径可以由铜逐步转变为氢氧化铜?
⑤铁与硫酸铜溶液可以反应,钠可以吗?
【查阅资料与问题解决】
(1)铜不能与稀硫酸发生置换反应,是因为在金属活动性顺序表中,铜排在
之后.
铜能与浓硫酸发生反应,其反应方程式为:Cu+2H
2SO
4(浓)
CuSO
4+2H
2O+SO
2↑
此反应中化合价升高的元素是
.
(2)铜在潮湿的空气中能通过化合反应“生锈”形成铜绿,铜绿的主要成分为Cu
2(OH)
2CO
3.由此可以推测:铜“生锈”过程中,参与反应的物质有铜、水和
.
(3)氧化铜不能与水反应生成氢氧化铜,但可以在加热的条件下被一氧化碳等还原成铜,也能与硫酸、盐酸等反应形成相应的铜盐和水,请写出氧化铜与稀硫酸反应的化学方程式:
;在高温下,氧化铜能分解成砖红色的氧化亚铜(Cu
2O)和氧气,反应的化学方程式为:
.
(4)同学们设计了以下装置(夹持、尾气处理装置装置未画出),实验中观察到黑色固体变为红色物质,无水CuSO
4变蓝色,同时生成一种无污染的气体.
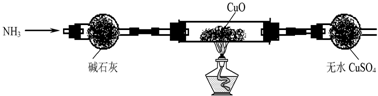
证明CuO能被NH
3还原.该反应的化学方程式为
.
(5)资料显示:甲烷具有还原性,可以还原氧化铜,生成CO
2和H
2O.同学们对此提出了质疑并进行探究.同学们用纯净的甲烷气体和如下装置进行实验.
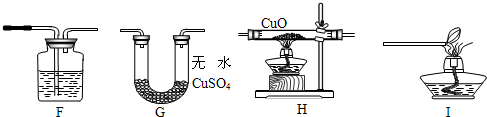
①上图装置F中盛放的试剂名称是
.
②上图装置的正确连接顺序是
(填字母,且每套装置限用一次).
③甲烷还原氧化铜的化学方程式为:
.
(6)由铜转化为氢氧化铜,从化学反应的原理看,可以是流程I:
Cu
CuSO
4Cu(OH)
2也可以是流程II:
Cu
CuO
CuSO
4Cu(OH)
2与流程I相比,流程Ⅱ的优点是
.
(7)某化学兴趣小组把金属钠投到硫酸铜溶液中,实验并非如想 象的有红色铜析出,而是生成一种蓝色沉淀.实验中到底发生了怎样的化学反应?同学们非常好奇并进行实验探究.
【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体
【提出猜想】钠先与水反应生成某气体和溶液,该溶液再与硫酸铜反应生成蓝色沉淀;
【实验探究】实验一:同学们把一小块钠投到装有少量蒸馏水的试管中,经验纯后点燃生成的气体,听到“噗”的一声后燃烧起来;
实验二:在剩余的溶液中加入硫酸铜溶液,发现有蓝色沉淀.
【实验总结】①水与金属钠反应的化学方程式
.
②请你判断猜想
(“成立”或“不成立”).

 碱式碳酸铜受热可生成氧化铜、水和二氧化碳,实验装置如图,试回答下列问题:
碱式碳酸铜受热可生成氧化铜、水和二氧化碳,实验装置如图,试回答下列问题:

 阅读快车系列答案
阅读快车系列答案


 乙炔俗称电石气,是因为电石(CaC2)遇水可产生乙炔(C2H2)气体,反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑某桶电石标签的部分内容如图所示.计算:
乙炔俗称电石气,是因为电石(CaC2)遇水可产生乙炔(C2H2)气体,反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑某桶电石标签的部分内容如图所示.计算: